[이데일리 김지완 기자] 한 주(12월13일~12월17일) 국내 증권사에서 발간한 주요 제약·바이오 보고서다.
 | | [이데일리 노진환 기자] 제5회 이데일리 글로벌 제약바이오 콘퍼런스가 7일 오후 서울 중구 KG타워에서 개최됐다. 김태규 바이젠셀 대표가 ‘플랫폼 기반의 면역세포 치료제 개발’을 주제로 발표하고 있다. |
|
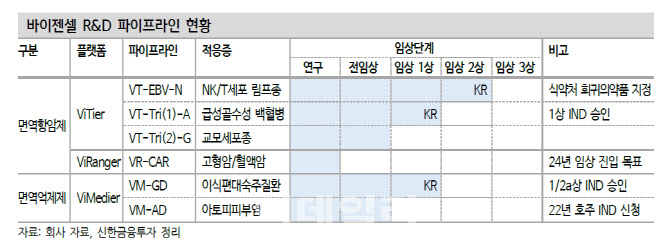
바이젠셀, R&D 순항 중 신한금융투자는 지난 15일 ‘바이젠셀, R&D 계획대로 순항 중’이라는 보고서를 냈다.
우선 임상 2상이 예정대로 진행 중이라는 진단이다. 장세훈 책임연구원은 “NK/T 림프종 국내 임상 2상 진행 중인 리드 파이프라인 ‘VT-EBV-N’은 환자 모집이 65% 정도 진행된 상황”이라며 “내년 상반기까지 환자 모집이 완료할 예정이고 오는 2024년 상반기 임상이 완료될 전망”이라고 내다봤다.
해외 사업 확대와 기술수출을 통해 기업가치 확대를 꾀하고 있다는 점도 긍정적이다. 바이젠셀은 VT-EBV-N은 중국 합자회사(JV) 설립을 통한 개발 파트너십을 목표로 사업개발을 진행하고 있다. 또 호주 현지 법인 설립을 통해 바이레인저와 바이메디어의 글로벌 임상 데이터를 확보해 기술 이전 역량을 높일 계획으로 전해졌다.
장 연구원은 “CAR-T를 비롯해 세포 치료제에 대한 글로벌 기업들의 관심도는 여전히 유효하다”며 “바이젠셀은 3가지 차별화된 세포치료제 플랫폼을 보유하고 있어 향후 사업개발 전략을 통한 글로벌 개발 파트너십을 기대할 수 있다”고 말했다.
이날 신한금융투자는
바이젠셀(308080)에 대해 별도의 투자의견이나 목표주기를 제시하지 않았다.
보령제약, BR2002 기대감↑ 이베스트투자증권은 지난 15일 ‘보령제약, BR2002 결과...나쁘지 않다’ 보고서를 냈다.
보령제약은 13일(현지시간) 미국 혈액학회(American Society of Hematology, ASH)에서 자체 항암신약인 비호지킨성 림프종 치료제 ‘BR101801’(프로젝트명 BR2002) 임상 1a상 결과를 발표했다. 이 치료제는 암세포의 주요 성장인자인 PI3K 감마, PI3K 델타, 그리고 DNA-PK를 동시에 삼중 저해하는 비호지킨성 림프종 치료제다. 임상 1a상은 한국과 미국에서 동시에 진행됐다.
보령제약이 발표한 결과에 따르면, 총 9명의 말초 T세포 림프종(Peripheral T-Cell Lymphoma, PTCL) 환자 중 1명에게서 암세포가 모두 사라진 상태의 ‘완전관해’, 2명에게서는 ‘부분관해’를 확인했다. 투여 2개월 차에 2명의 환자에서 부분관해가 확인됐고, 이후 추가적으로 다른 1명에게서 투여 5개월 차에 부분관해가 확인됐다. 이 환자는 9개월 차에 암세포가 모두 사라졌다.
강하나 연구원은 “항암치료에서 가장 중요한 지표 중 하나인 PFS(무진행생존기간) 중앙값은 11.1개월로 유의미한 결과를 냈다”며 “이에 따라 PTCL환자군을 대상으로 임상1b/2상을 동시에 진행해 나갈 예정이다. 희귀의약품 특성상 높은 성공률, 빠른 조건부허가를 통한 임상승인을 기대해볼 수 있다”고 평가했다.
그는 “임상 초기 단계에서 그레이드 4(Grade 4) 이상의 부작용도 없었던 만큼 T세포 림프종에 대한 우수한 효능과 안전성을 확인했다는 점에서 의미가 있다”며 “PI3K 저해제 항암제 중 글로벌리 가장 관심을 많이 받고 있는 베라스템온콜로지의 혈액암 치료제 코픽트라(두벨리십)가 PI3K 델타와 감마를 이중 억제하는 최초 기전의 약물 이후의 퍼스트인 클래스(FIRST-IN-CLASS)로서 삼중저해를 해낼 기전이라는 데에서 관심을 가져볼 만하다는 판단”이라고 부연했다.
이날 이베스트투자증권은
보령제약(003850)에 대해 투자의견 매수를 제시하고 목표주가 2만원을 제시했다.




![로킷헬스케어 1.9조 수주 계약이라더니…구속력 無·매출 전환율 0.8%[only 이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/05/PS26050400118b.jpg)