[이데일리 김진호 기자]면역 T세포치료제 전문기업
바이젠셀(308080)은 ‘바이티어’와 ‘바이레인저’, ‘바이메디어’ 등 크게 세 가지 종류의 T세포 생산 및 개발 플랫폼을 보유하고 있다. 이를 통해 회사가 현재까지 발굴한 주력 후보물질(파이프라인)은 총 8종이며, 암 및 자가면역질환 등의 적응증으로 개발하는 중이다.
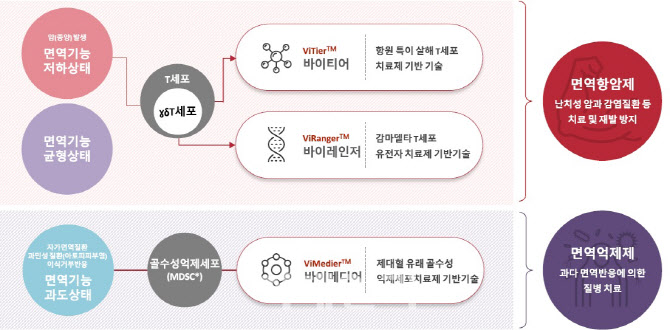 | | 바이젠셀이 보유한 세 가지 세포치료제 개발 플랫폼 ‘바이티어’, ‘바이레인저’, ‘바이메디어’ 개요.(제공=바이젠셀) |
|
바이젠셀, 종류별 T세포 생성 플랫폼 확보 김태규 바이젠셀 대표는 1990년대 중반부터 가톨릭대 의대에서 연구자 주도 T세포치료제 시도한 전문가다. 그가 과거 연구 내용과 성과를 바탕으로 설립한 회사가 바이젠셀이다.
김 대표에 따르면 우리 몸의 T세포의 90%가 표면에 알파베타(αβ) 수용체를 발현하고 있는 αβ T세포다. 업계에서 일반적으로 쓰는 T세포는 사실 αβ T세포를 줄인 표현이다. αβ T세포의 대부분이 표면에 CD8 단백질을 가진 세포독성T세포(CTL)이며, 그 외에 도움 T세포나 조절 T세포 등도 여기에 포함된다.
바이젠셀이 초창기 내세운 것이 ‘바이티어’는 세포성 면역에 관여하는 세포독성T세포 분리배양하는 기술이다. 김 대표가 1998년 NK/T세포 림프종 환자 3명에게 연구자 주도 임상을 시도한 것도 세포독성T세포 치료제였다. 해당 치료제가 바로 현재 회사의 주력 후보물질 ‘VT-EBV-N’이며 국내에서 상업화를 위한 임상 2상을 진행하고 있다.
이밖에 바이레인저와 바이메디어는 각각 체내에 소량 존재하는 감마델타 T세포(γδ T세포)와 제대혈 유래 골수성 억제세포를 확보하는 기술이다. 특히 바이젠셀은 “바이메디어가 세계적으로도 보기 드문 기술”이라고 자신하고 있다.
김 대표는 “제대혈에 있는 혈액 줄기세포에 여러 신호전달 물질을 가해 골수성 억제세포 분화시킬 수 있다. 일반적으로 알려진 것보다 10배 이상의 해당 세포를 얻는 기술을 보유하고 있다”며 “바이레인저와 바이메디어 플랫폼은 희소성이 있는 플랫폼이다”고 운을 뗐다.
그는 이어 “비교적 업계에서 생소한 골수성 억제세포의 경우 고형암이 있는 주변 지역에서 T세포의 활성을 억제하는 역할을 한다. 종양의 성장을 돕는 것이다”며 “이를 역이용해 T세포 과활성으로 인한 자가면역질환인 아토피 피부염이나 이식편대숙주질환(GVHD) 등 적응증을 타깃하는 물질을 개발하려는 중이다”고 말했다.
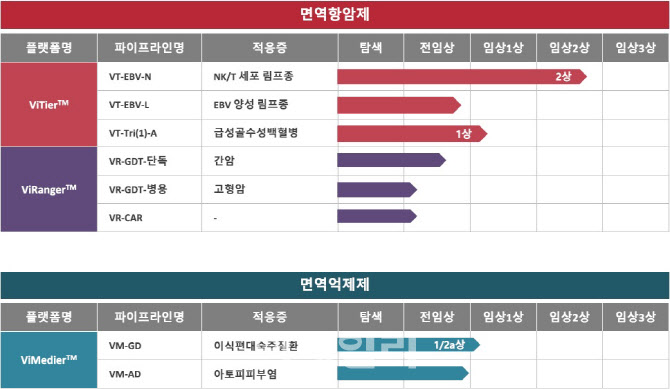 | | 바이젠셀의 주요 후보물질 개발 현황(제공=바이젠셀) |
|
“‘세포치료제→세포유전자치료제’로 변신할 계획” 바이젠셀은 앞서 언급한 NK/T세포 림프종 치료제 후보물질 ‘VT-EBV-N’(임상 2상)과 급성골수성백혈병 치료제 후보물질 ‘VT-Tri(1)-A’(임상 1상) 등은 바이티어 플랫폼 기반 임상 진입에 성공한 물질이 2종이다. 여기에 바이메디어를 통해 발굴한 이식편대숙주질환 신약 후보 ‘VM-GD’의 임상 1/2a상도 지난 2020년 11월 식품의약품안전처로부터 승인받았다.
김 대표는 “가장 빠른 VT-EBV-N은 적응증도 희귀질환이기 때문에 2상 결과로 조건부 허가를 신청할 수 있다”며 “중국이나 일본 등에 있는 일부 기업들과 이에 대한 기술수출 논의도 하고 있는데, 국내 시판 상황까지 보겠다는 조율을 하자는 입장이다”고 말했다. VT-EBV-N이 국내 시판에 성공하면 아시아 시장 진출 시도가 빠르게 진행될 수 있다는 얘기다.
이외에도 회사는 △바이티어 기반 ‘VT-EBV-L’(EBV 양성 림프종) △바이레인저 기반 ‘VR-GDT’(간암 대상 단독 및 고형암 대상 병용요법)과 ‘VR-CAR’(적응증 미정) △바이메디어 기반 ‘VM-AD’(아토피 피부염) 등 신규 후보물질에 대해 다섯 가지 적응증을 타깃하는 전임상 연구를 병행하고 있다.
한편 바이젠셀은 세포치료제에서 세포유전자치료제(CGT)로 영역을 확장하려는 시도를 지속할 계획이다. 회사는 지난해 4월 바이젠셀이 미국암학회(AACR)에서 내놓은 ‘VR-CAR’의 전임상 결과가 그 밑거름이 될 것으로 분석하고 있다.
VR-CAR는 CD30 자극하는 영역(도메인)을 포함한 γδ T세포이며, 바이젠셀은 이 세포가 여러 고형암 동물 모델에서 암세포를 억제했다는 전임상 결과를 획득했다. CD30에 유전자 변형을 거쳐 고형암을 타깃하는 유전자 변형 세포치료제로도 활용될 여지가 있다는 분석이다.
김 대표는 “시판 중인 CAR-T치료제의 가장 큰 한계가 자가로 만들어 범용성이 떨어진다는 것과 고형암에서 효과가 확인되지 않았다는 것이다”며 “γδ T세포는 NK세포와 T세포의 특징을 보유하고 있다. 고형암에서도 효능을 확인한 만큼 유전자 변형을 거쳐 이를 극대화하는 연구를 수행해 내후년에는 임상에 진입하도록 만들 계획이다”고 말했다.
그는 이어 “세포치료제로 개발을 시도하고 있지만, 효과를 극대화하기 위해 유전자 변형은 이제 필수 옵션이라고 생각한다”며 “기존 후보물질의 임상과 생산을 안정화하면서 CGT 전문회사로 변모할 수 있도록 역량을 확보해 나가겠다”고 덧붙였다.