[이데일리 신민준 기자] 세포치료제 전문기업인
테고사이언스(191420)가 올해 일본 등 해외시장 진출을 통해 성장에 박차를 가한다. 테고사이언스는 세계에서 가장 많은 종류의 세포치료제 상용화에 성공한 기업으로 국내를 벗어나 해외시장에서 진검승부를 벌인다.
테고사이언스는 일본의 경우 기존 제품인 2도 화상 등 동종유래 줄기세포치료제 칼로덤, 미국은 바이오 신약 회전근개파열 치료제 ‘TPX-115’를 앞세운 투트랙 전략으로 시장 공략에 나선다는 방침이다. 테고사이언스는 올해 첫 매출 100억원 돌파가 예상된다.
 | | (그래픽=이데일리 김일환 기자) |
|
日, 세포치료제 인허가 우호적…약 2000억원대 시장 공략 21일 바이오업계에 따르면 테고사이언스는 연내 대표 제품 칼로덤의 일본 후생노동성(PMDA)를 인허가를 신청할 예정이다. 테고사이언스는 일본 파트너사인 메이저 바이오기업과 인허가 신청 시기 등을 협의하고 있다. 칼로덤이란 미리 적출한 다른 사람의 세포를 배양해 다수의 환자에게 적용할 수 있는 동종유래피부각질(표피) 세포치료제를 말한다. 칼로덤은 환자에게 언제든지 바로 적용할 수 있는 장점이 있다. 칼로덤은 미색의 투명한 막 형태인 피부각질세포시트가 바셀린 거즈에 부착돼 연한 노랑에서 빨강색을 띄는 보존액과 함께 흰색 폴리스티렌 용기에 냉동보관돼 있다.
칼로덤은 피부 화상을 입어 수포가 생기는 2도 화상과 발 등 당뇨병을 가진 사람에게 발생하는 궤양인 당뇨병성족부궤양 환자에게 적용된다. 칼로덤은 산재보험과 건강보험을 받아 환자들의 경제적인 부담도 덜어준다. 칼로덤은 상처부위에 주변부효과를 통해 줄기세포를 상처부위로 이동하도록 유도하고 이들의 증식을 촉진해 상처를 치유한다. 칼로덤을 단독으로 적용하거나 이식피부 등과 병용해 사용할 수 있다. 칼로덤은 2005년 국내 최초 동종유래 세포치료제로 식약처의 제품허가 승인을 받았다.
테고사이언스가 일본시장을 겨낭하는 이유는 국내 시장보다 시장 규모가 큰데다 칼로덤과 같은 동종유래세포치료제가 아직 없기 때문이다. 한국IR협의회 기업리서치센터에 따르면 일본은 환자의 세포를 직접 사용해 세포를 분리 배양해 환부에 이식하는 재생의료전문기업 제이텍(J-TEC)의 자기유래세포치료제 제품이 약 200억원 규모로 판매되고 있다.
칼로덤이 동종세포치료제를 포함해 공략할수 있는 일본시장 규모는 약 2000억원으로 추정된다. 칼로덤은 국내에서 약 70억원의 매출을 발생시키고 있다. 칼로덤은 2005년 국내에서 출시돼 안정·유효성을 확인한 만큼 일본시장에 빠르게 진입할 것으로 예상된다. 일본이 세계적으로 세포치료제 허가에 우호적인 국가 중 하나라는 점도 긍정적인 부분이다.
테고사이언스는 미국시장 진출도 서두르고 있다. 테고사이언스는 회전근개부분파열 동종유래섬유아(진피) 세포치료제의 ‘TPX-115’ 미국 임상 2상을 준비하고 있다. 회전근개는 어깨 부위 4개 근육과 어깨뼈와 이를 연결해주는 건(Tendon)를 통칭한다. 회전근개 파열은 무리한 운동아니 오화 등의 요인으로 인해 어깨와 팔을 연결하는 근육과 인대가 강한 외부 충격에 손상돼 통증을 유발하는 대표적인 퇴행성 질환이다. 테고사이언스는 섬유아세포치료제를 통해 콜라겐 등 세포외기질을 합성함으로써 파열된 회전근개 구조를 재건하는 근본적인 치료법 제시를 목표로 하고 있다.
테고사이언스는 미국 임상 2상 이후 임상 3상도 진행할 예정이다. 이를 위해 테고사이언스는 현지 조인트벤처(JV) 설립도 검토 중이다. TPX-115는 이르면 2026년 미국 임상 3상을 완료하고 제품 허가를 신청할 수 있을 것으로 기대하고 있다. 리서치앤마켓에 따르면 전 세계 회전근계파열 시장 규모는 2022년 9억6100만달러(1조3000억원) 에서 2030년 15억2700만달러(약 2조원) 규모로 연평균 6% 성장이 전망된다.
테고사이언스 관계자는 “자사는 그동안 인도네시아 등의 국가에 도의적인 목적으로 긴급하게 일부 칼로덤 등의 제품을 수출했지만 상업화인 수출을 하지 못한 측면이 있었다”며 “올해가 본격적인 제품 수출의 원년으로 큰 수익이 발생할 수 있는 터닝포인트로 보고 있다”고 말했다.
세계서 가장 많은 세포치료제 상용화 성공 테고사이언스는 국내 세포치료제시장 공략에도 공을 들이고 있다. 테고사이언스는 2002년 식품의약품안전처의 제품 허가 승인을 받은 홀로덤이 국내 환자들에게 꾸준히 사용되고 있다. 홀로덤은 3도 이상 중증 화상 환자 치료를 위한 자기유래피부각질 세포치료제로 2007년부터 산재보험의 적용을 받았다.
테고사이언스는 회전근개파열 자기유래섬유아 세포치료제 ‘TPX-114’의 국내 임상 3상도 진행 중이다. TPX-114의 국내 임상 3상은 연내 마무리될 것으로 예상된다. 테고사이언스는 눈밑주름(비협골고랑)의 개선을 적응증으로 하는 자기유래섬유아세포치료제 로스미르를 개발해 2017년 식약처에서 제품 허가를 받았다.
로스미르는 국내 최초로 주름 개선 적응증으로 식약처의 제품허가를 받았다. 로스미르 피부진피층을 구성하고 있는 섬유아세포를 투여해 생리활성물질, 콜라겐과 같은 세포외기질 합성을 촉진해 피부구조를 유지하고 복구하는 효능을 나타낸다. 테고사이언스는 로스미르의 동종유래섬유아 세포치료제 ‘TPX-121’이 전임상시험 단계에 있다. TPX-121은 이르면 연내 임상 1상 신청이 예측된다.
이밖에 3차원 배양피부인 네오덤도 테고사이언스가 기대하는 제품이다. 네오덤은 인간의 피부세포를 테고사이언스의 세포배양기술을 적용해 제조하며 사용목적에 따라 여러 층과 세포의 조합으로 제조할 수 있다. 네오덤은 진피와 표피를 재현한 실험용 피부모델로서 의약품과 화장품 원료의 안전·유효성 평가에 사용되고 있다. 특히 세계적으로 동물실험금지를 위한 입법화가 추진되고 있어 수요 증가가 예상된다.
테고사이언스는 홀로덤, 칼로덤, 로스미르 등 3개의 세포치료제를 상용화에 성공했다. 이는 세계적으로 가장 많은 수치로 상용화에 성공한 세포·유전자 치료제 30여개에 이른다. 밑바탕에는 테고사이언스가 보유한 기술력이 있다. 테고사이언스는 2001년 설립 이후 20여년간 세포치료제 개발에 전념하고 있다.
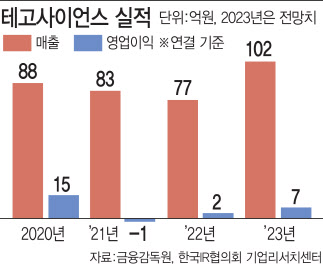
테고사이언스는 자체 보유한 우수의약품·제조품질관리기준(GMP) 생산시설에서 세포치료제 제조와 위탁개발생산(CDMO) 사업을 진행하고 있다. 테고사이언스는 해외 진출에 힘입어 실적 개선이 기대된다. 올해 매출은 102억원, 영업이익은 7억원이 추정된다.
박선영 한국IR협의회 기업리서치센터 연구원은 “테고사이언스는 홀로덤과 칼로덤 등의 캐쉬카우 제품들을 바탕으로 이미 재무적 성과를 달성하고 있다”며 “지난해 기준 순현금 약 211억원으로 견고한 재무 안정성도 보유했다. 칼로덤의 일본 수출 등 해외 매출 확대로 기업가치 재평가가 이뤄질 것”이라고 말했다.