[이데일리 송영두 기자] 지난해와 올해에 걸쳐 마이크로바이옴 신약이 승인되면서 새로운 전기가 마련하고 있습니다. 승인된 신약은 물론 대부분의 국내외 마이크로바이옴 치료제 개발 기업들은 감염병 치료제 개발에 나서고 있습니다. 하지만 최근에는 마이크로바이옴 항암제 개발에 높은 투심이 이어지면서 새로운 시장에 관심이 집중되고 있습니다.
한국바이오협회 ‘마이크로바이옴 투자 및 산업동향’ 리포트에 따르면 마이크로바이옴 투자는 2021년부터 강한 상승세를 보였습니다. 2022년에도 비슷한 양상을 보이며 한 해 동안 18억 유로(약 2조4500억원)이 투자됐습니다. 이 중 흥미로운 것은 마이크로바이옴 치료제 투자 분야의 미묘한 변화입니다.
2021년 감염병을 적응증으로 한 치료제 분야에 약 4억4000만 유로(약 6257억원)가 투자돼 가장 높은 규모를 형성했습니다. 하지만 2022년에는 감염병에 대한 투자가 크게 감소한 반면, 항암 분야 투자가 약 5억 유로(약 7110억원)로 늘어나면서 가장 높은 투자 규모를 나타냈습니다.
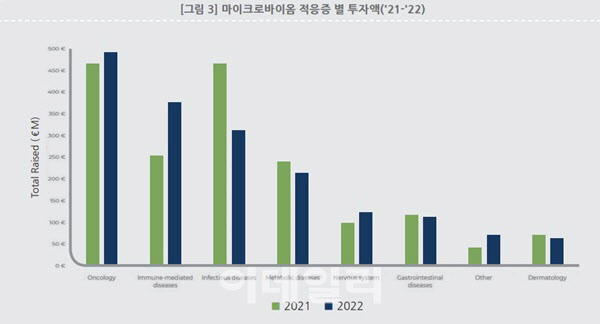 | | (자료=한국바이오협회) |
|
실제로 일부 마이크로바이옴 치료제 기업들은 감염병 외 항암제 분야로 눈을 돌려 개발에 나서고 있습니다. 프랑스 제약사 엔테롬 바이오사이언스는 BMS와 면역항암제 공동개발에 나서고 있고, 니볼루맙 병용 임상 1/2상에서 긍정적인 임상 결과를 확인했습니다. 영국 4D파마는 고형암 치료제 임상 1상을 진행 중이고, 미국 신로직 역시 고형암 1상을 진행 중입니다. 또 미국 베단타 바이오사이언스도 고형암 1상을, 미국 세컨드지놈은 고형암 전임상 연구개발을 진행 중입니다.
국내의 경우
지놈앤컴퍼니(314130),
CJ(001040)바이오사이언스,
쎌바이오텍(049960), MD헬스케어가 마이크로바이옴 항암제 개발에 착수한 상태입니다. 눈여겨봐야 할 점은 마이크로바이옴 항암제 개발 분야에서 한국 기업의 활약입니다. 현재 마이크로바이옴 면역항암제 개발에 있어 글로벌 선두 그룹은 4D파마, 베단타, 신로직과 함께 지놈앤컴퍼니가 꼽힙니다. 지놈앤컴퍼니는 위암과 담도암 치료제를 개발 중인데, 모두 임상 2상 중으로 개발 속도가 가장 빠릅니다.
특히 지놈앤컴퍼니는 마이크로바이옴 치료제 기업 최초로 임상 2상에서 유효성을 입증했습니다. 지난 5월 면역항암 마이크로바이옴 치료제 ‘GEN-001’과 바벤시오(성분명 아벨루맙) 위암 병용 요법 임상 2상 중간 분석 목표를 성공적으로 달성했습니다. GEN-001과 바벤시오(성분명 아벨루맙) 위암 병용 임상 2상 중간 분석 결과 기존 경쟁 치료제 대비 우수한 객관적 반응률(ORR)을 입증했습니다.
 | | 자놈앤컴퍼니 마이크로바이옴 면역항암제 개발 현황.(자료=지놈앤컴퍼니) |
|
지놈앤컴퍼니의 임상 2상 중간 분석 목표는 ORR 5% 이상인데, 이를 상회하는 수준으로 확인됐습니다. 이에 따라 미국 독립적 데이터 모니터링 위원회(IDMC)가 ‘GEN-001’의 위암 대상 임상 2상을 기존 계획대로 계속 진행하라고 의견을 냈습니다. 윤영광 지놈앤컴퍼니 연구개발 그룹장은 “이번 결과는 면역항암 분야 세계 최초로 임상 2상에서 유효성과 안전성을 입증할 수 있는 결과를 도출했다는 의미가 있습니다”라며 “면역항암 마이크로바이옴 치료제 개발 가능성을 입증한 것입니다”라고 강조했습니다.
GEN-001은 건강한 사람의 장에서 분리 동정한 락토코쿠스 락티스(Lactococcus lactis) 균을 활용해 체내 선천면역 및 적응면역 활성화 작용 기전을 갖고 있습니다. 이를 통해 PD-(L)1 억제제 내성 및 불응성 고형암 치료 효능을 나타냅니다. 경구용 제제로 우수한 면역항암 효능은 물론 타 면역항암제 병용약물 대비 부작용이 적다는 것도 큰 장점으로 꼽히고 있습니다.
지놈앤컴퍼니의 이런 성과는 스위스 페링제약이 세계 최초 마이크로바이옴 치료제 개발에 성공한 것만큼, 큰 의미가 있다는 게 업계 분석입니다. 마이크로바이옴 항암제 가능성을 지놈앤컴퍼니가 세계 최초로 입증했기 때문입니다. 최종적으로 임상 2상 완료 후 유효성 데이터를 도출하게 되면 마이크로바이옴 항암 신약의 새로운 역사를 한국 기업이 쓰게 될 가능성이 매우 높은 상황입니다.
이미 글로벌 제약사 독일 머크-화이자와 MSD는 지놈앤컴퍼니의 면역항암제 개발 가능성에 공동개발에 나선 상황입니다. 지놈앤컴퍼니 측은 GEN-001 위암 대상 임상 2상 데이터를 확보하고, 기술이전에 나선다는 계획입니다.
또한 지놈앤컴퍼니는 최근 ‘GEN-001’ 담도암 대상 임상 2상에서 첫 환자 투여를 완료했습니다. GEN-001 담도암 대상 임상 2상은 MSD 면역항암제 키트루다(성분명 펨브롤리주맙)와 병용투여로 진행됩니다. 이전 치료에서 효과를 보지 못한 담도암 환자를 대상으로 국내 8개 병원에서 이뤄집니다. 해당 임상을 통해 병용투여에 대한 안전성 및 유효성을 입증할 계획입니다.