팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 신민준 기자] 신약 개발 전문기업
브릿지바이오테라퓨틱스(288330)(브릿지바이오)가 올해 흑자전환을 노린다. 브릿지바이오는 지난 2019년 코스닥 기술 특례 상장 이후 4년째 영업적자(손실)를 기록하고 있다.
브릿지바이오는 연내 글로벌 임상 2상을 진행 중인 계열 내 최초 경구용 오토택신 저해제이자 특발성 폐섬유증 치료제의 기술 이전(수출)을 통해 실적 반전을 꾀한다. 특히 브릿지바이오는 특발성 폐섬유증과 4세대 비소세포폐암 표적치료제 두 가지 주력 신약 파이프라인 개발 및 기술이전 등에 전사 역량을 집중한다.
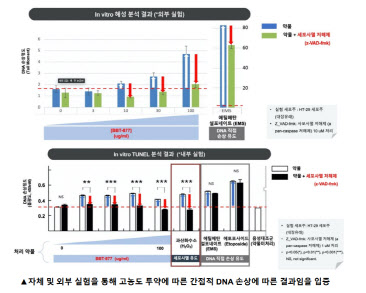 | | BBT-877 위약성 확인 실험 결과.(자료=브릿지바이오 테라퓨틱스) |
|
권리 반환 폐섬유증 치료제 잠재적 독성 이슈 해소 8일 바이오업계에 따르면 브릿지바이오는 지난해 매출 1억원, 영업손실 403억원을 기록했다. 매출은 전년(30억원) 대비 크게 감소했다. 브릿지바이오의 수익원은 기술 이전을 통한 계약금과 마일스톤(기술료)이다. 브릿지바이오는 신약 후보물질을 직접 발굴하지 않고 외부에서 도입해 개발에 집중해 빠르게 임상 단계를 끌어올리는 임상개발특화(NRDO) 전략을 펼치고 있다. 그 결과 브릿지바이오는 2019년 임상 1상 단계의 특발성폐섬유증 치료제 후보물질 ‘BBT-877’을 독일 베링거인겔하임에 약 1조5000억원 규모로 기술 이전했다. 하지만 베링거인겔하임이 이듬해인 2020년 혜성 분석(Comet assay) 결과 잠재적 독성의 우려가 있다며 권리를 반환했다.
혜성분석은 약물에 의한 유전자(DNA) 손상 여부를 살피는 실험의 일종으로 약물 처리에 의해 DNA 손상이 있는 경우 세포핵이 현미경에서 혜성과 같은 모양을 나타내게 된다. 이러한 혜성 분석에서 양성 결과가 나올 경우 약물 자체의 유전 독성에 의한 직접적인 DNA 손상으로 발암 가능성이 있을 수 있다.
브릿지바이오는 베링거인겔하임의 혜성 분석이 위양성(False positive·가짜 양성)일 것이라고 판단하고 내·외부 실험을 단행했다. 브릿지바이오는 자체 실험 결과 BBT-877의 혜성 분석 양성결과가 약물의 유전 독성으로 DNA의 직접적인 손상이 아닌 고농도 약물인 세포사멸 저해제에 의한 세모 사멸로 발생한 DNA의 간접적인 손상이라는 점을 확인했다.
브릿지바이오의 자체 실험 결과 에틸메탄설포네이트와 에토포사이드 등 직접적으로 DNA에 손상을 가하는 약물은 세포사멸 저해제의 영향을 받지 않았다. 하지만 BTT-877은 세포사멸 저해제의 영향을 받았다. 브릿지바이오는 외부기관인 미국 보스턴 엠비바이오사이언스 실험에서도 동일한 결과를 얻었다.
브릿지바이오 관계자는 “브릿지바이오는 권리 반환 이후 내·외부 위탁 실험들을 추가로 수행하여 BBT-877의 혜성 분석 양성결과가 약물의 유전 독성으로 DNA의 직접적인 손상에 따른 진양성(True Positive·진짜 양성)이 아니라는 점을 입증했다”며 “고농도 약물 처리 세포사멸 저해제에 의한 세포 사멸로 DNA 간접 손상 즉 위양성에 해당했다”고 설명했다.
브릿지바이오는 2022년 초 미국 식품의약국(FDA)에 BBT-877의 자체 개발 글로벌 임상 2상을 다시 신청했고 같은 해 7월 FDA의 허가를 받았다. 브릿지바이오는 기술 반환의 이유가 잠재적인 독성 문제였던 만큼 규제 기관에서 임상을 허가하면서 우려됐던 부분이 해소됐다고 밝혔다. 특발성 폐섬유증은 알 수 없는 원인으로 과도하게 축적된 콜라겐 섬유조직으로 폐가 서서히 굳어지면서 기능을 상실하는 희귀질환이다. 최근 급속한 노령화와 코로나 후유증 등으로 관련 환자가 지속해서 증가하는 추세다.
특발성 폐섬유증은 현재 치료제 개발을 위해 많은 임상 연구가 진행되고 있지만 아직 질병을 완치할 수 있는 치료제가 없어 미충족 의료 수요가 매우 많다. 글로벌 시장조사기관 리서치앤마켓에 따르면 전 세계 특발성 폐섬유증 치료제 시장은 매년 7%의 높은 성장률을 보이며 2020년 기준 31억 달러(약 4조원)에서 오는 2030년에는 약 61억 달러(약 8조원)로 성장할 전망이다.
BBT-877과 같은 오토택신 저해제 계열로 개발되고 있던 벨기에 갈라파고스사의 특발성 폐섬유증 치료제 ‘GLPG1690’이 임상 3상 중 약물의 효용·위험도 관련 이슈로 임상을 중단해 계열 내 최초 약물(First-In-Class)로 올라선 점도 브릿지바이오에 호재로 작용할 전망이다. 브릿지바이오는 내년 상반기 중 BBT-877의 임상 2상 톱라인(주요 지표) 데이터를 공개할 예정이다. 브릿지바이오는 지난 1월 미국 캘리포니아주 샌프란시스코에서 개최된 ‘2024 JP모건 헬스케어 컨퍼런스’에 참가해 BBT-877의 기술 이전을 위해 다국가 제약사 5곳과 만난 뒤 현재 후속 협의 단계를 진행 중으로 알려졌다.
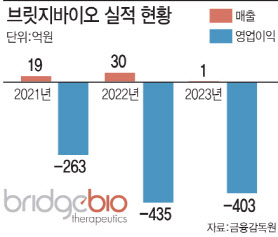 | | (그래픽=이데일리 문승용 기자) |
|
심장판막 질환 등 적응증 확장…신약 파이프라인 선택과 집중 브릿지바이오는 BBT-877의 적응증도 확장한다. 브릿지바이오는 BBT-877의 심장 판막 질환 적응증 추가를 위한 비임상 연구 결과를 국제 의학 학술지 바이오메드센트럴 메디신에 게재했다. 공개된 결과에 따르면 대동맥판막 협착증이 유도된 쥐에서 BBT-877 투약군은 72% 수준까지 석회화를 억제했다. BBT-877은 판막 조직의 섬유화 역시 약 80% 억제하며 대조군과 유사한 수준으로 조절된 것을 확인했다.
브릿지바이오는 4세대 폐암 표적치료제 후보물질 ‘BBT-207’의 국내 임상 1/2상을 진행 중이다. BBT-207은 비소세포폐암 환자에서 3세대 상피세포성장인자수용체(EGFR) 저해제 치료 이후 내성으로 나타나는 C797S 양성 이중 돌연변이 등을 선택적으로 저해하는 4세대 상피성장인자수용체 티로신 인산화효소 억제제(EGFR TKI)로 개발하고 있다. 브릿지바이오는 BBT-207의 비임상 실험 결과 비소세포폐암에서 3세대 EGFR 저해제로 1차 치료 후 발생할 수 있는 C797S를 포함해 이중 돌연변이를 비롯한 삼중 돌연변이에 대해 경쟁력 있는 수준의 항종양 효력을 확인했다. 앞서 브릿지바이오는 폐암 치료제로 개발하던 ‘BBT-176’과 안저질환 치료제 후보물질 ‘BBT-212’ 신약 파이프라인을 정리했다.
브릿지바이오 관계자는 “브릿지바이오는 BBT-877과 BBT-207 두 가지 신약에 전사 역량을 집중하고 있다”며 “브릿지바이오는 연내 최대한 BBT-877의 기술 이전을 통해 흑자전환을 시키도록 최선을 다하겠다”고 말했다.






![고영, 어닝서프라이즈에 '上'…바이젠셀·툴젠도 상승세[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042700146b.jpg)


![[임상 업데이트] 샤페론, 누겔 美 FDA 임상 2b상 투약·추적 관찰 완료](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042500203b.jpg)