[이데일리 김새미 기자] 올해 4분기에는 손익분기점(BEP)에 도달할 것이라던 뷰노(338220)가 BEP 도달 예상 시점을 내년 1분기로 한 분기 미뤘다. 주요 제품인 ‘뷰노메드 딥카스’(VUNO Med-DeepCARS, 이하 딥카스)의 국내 매출 증가만으로도 내년이면 흑자 전환이 가능할 것이라는 자신감을 내비친 셈이다.
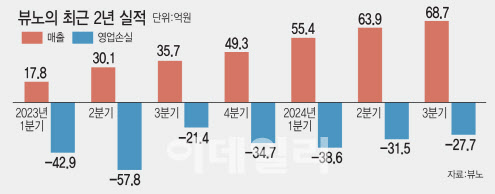
아쉬운 3분기 실적…의료 파업 장기화 영향? 25일 금융감독원 전자공시시스템에 따르면 뷰노의 3분기 매출은 69억원으로 전년 동기 대비 92.4% 증가했지만 영업손실이 28억원으로 29.4% 늘었다. 손실 폭이 오히려 늘어난 셈이다. 시장 추정치(컨센서스) 25억원보다 2억원 높은 영업손실을 기록하고, 매출 역시 추정치(82억원)보다 17%가량 낮게 나타났다.
 | | [그래픽=이데일리 김일환 기자] |
|
그럼에도 뷰노는 이번 분기 매출이 69억원이라는 것에 대해 ‘분기 최대 매출’이라고 의미를 부여했다. 지난해부터 7분기 연속 매출이 증가했으며, 해외 진출을 위한 일회성 비용 지출에도 불구하고 누적 기준으로는 영업손실이 감소했기 때문이다. 뷰노의 3분기 누적 영업손실은 98억원으로 전년 동기 122억원보다 19.9% 줄었다.
올 들어 영업비용은 매 분기 약 95억원씩 소모된 데 반해 매출 증가 속도가 예상보다 더뎠다. 현재로서는 뷰노의 매출이 대부분 국내에서 딥카스를 통해 발생하다보니 의료 파업이 장기화된 데 따른 영향이 컸을 것으로 추정된다.
뷰노의 주요 매출원인 예후·예측 솔루션 딥카스의 3분기 매출액은 59억원으로 전체 매출의 84.3%를 차지했다. 딥카스는 지난달 말 기준 상급종합병원 18개소를 포함한 97개소 병원에서 사용되고 있다. 8~9월에 부진했던 월매출이 지난달 들어 성장세를 보인 점은 긍정적인 요인이다. 뷰노는 최근 상급종합병원 2곳과 딥카스 도입에 대한 논의가 마무리되고 있다고 전했다. 빠르면 올해 4분기부터 딥카스 매출 증가에 기여할 것으로 기대된다.
회사는 딥카스에 대한 신의료기술평가 유예 기간 연장 소급 적용 관련해서도 큰 문제가 없을 것으로 예상하고 있다. 보건복지부가 신의료기술평가 유예 기간을 2년에서 최장 5년까지 연장할 경우 딥카스의 비급여 기간은 2027년 7월까지로 늘어나게 된다. 업계 관계자는 “(복지부가 신의료기술 평가 유예 기간 연장에 대한) 명문화 작업을 거의 완료한 걸로 알고 있다”고 언급했다.
매출 폭발시킬 美 진출, 내년으로 다가왔다 앞으로 뷰노의 매출이 폭발적으로 증가하기 위해서는 좁은 국내 시장을 벗어나 빠르게 미국 시장에 진출해야 한다. 국내 시장 규모는 연간 2965억원에 불과하기 때문이다. 반면 딥카스가 진출할 미국 시장의 규모는 연간 23억2000만달러(한화 약 2조7840억원), 유럽 시장은 연간 21억9500만달러(약 2조6340억원) 규모일 것으로 추정된다. 해외 진출이 매출 퀀텀점프의 기폭제가 될 것으로 기대되는 이유다.
딥카스는 지난해 6월 미국 식품의약국(FDA) 혁신의료기기(BDD)로 지정됐으며, 내년 상반기에 FDA 501(k) 인증을 획득해 내년 4분기부터 미국 매출이 발생할 것으로 기대된다. 특히 BDD로 승인 받았기 때문에 미국 시장에 경쟁사가 사실상 없을 것으로 예상된다. 미국 시장에서 뷰노의 경쟁자가 될 것이라고 지목되는 페라헬스(PeraHealth)의 심정지 예측 제품은 뷰노와 달리 인공지능(AI)이 적용되지 않았다.
딥카스보다 먼저 FDA 510(k) 승인을 받은 진단솔루션으로는 ‘뷰노메드 딥브레인’(VUNO Med-DeepBrain, 이하 딥브레인), ‘뷰노메드 체스트 엑스레이’(VUNO Med-Chest X-Ray)가 있다. 딥브레인의 경우 내년 상반기 가장 빨리 뷰노에 미국 매출을 안겨줄 진단솔루션이 될 것으로 예상된다. 체스트 엑스레이는 기업간거래(B2B) 제품이다 보니 시장 침투에 좀 더 시간이 걸릴 전망이다. 이외에 ‘하티브’(Hativ P30)도 내년 4분기 FDA 510(k) 승인을 목표로 내년 2분기 허가를 신청할 예정이다. 총 4개 제품을 기반으로 미국 시장을 공략하게 되는 셈이다.
뷰노는 미국 법인을 기반으로 현지 의료기관 대상 영업·마케팅을 강화해 시장 친출에 속도를 내겠다는 방침이다. 이를 위해 지난 6월 100% 자회사인 미국법인(VUNI MED Inc.)에 30억원 규모 주주배정 유상증자를 실시하기도 했다. 현지 시장 진입을 준비 중인 주요 제품의 임상·인허가 획득에 필요한 비용을 확보하기 위해서다.
회사 측은 해외 시장 진출에 따른 비용 증가 우려에 대해 연말까지만 관련 비용이 소모될 것이라고 일축했다. 뷰노 관계자는 “미국 진출에 따른 비용은 주로 임상과 인증에 대한 비용이라 일회성 비용이라고 보고 있다”며 “연말까지만 미국 진출에 따른 비용이 반영될 것”이라고 내다봤다.