팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 나은경 기자] 이종장기이식을 연구하는
옵티팜(153710)이 연내 완공을 목표로 무균돼지 생산시설을 새로 짓는다. 기존 무균돼지 생산시설을 강화될 가이드라인에 맞게 선제적으로 개조한 것인데, 돼지췌도이식 전임상에 본격적으로 대비하기 위한 것이라는 설명이다. 올해에서 내년으로 연기됐던 돼지췌도이식 전임상 진입도 머지 않은 것으로 보인다.
13일 제약·바이오 업계에 따르면 옵티팜은 지난 4월 기존 원균제어시설(DPF)의 리모델링 공사에 착수했다. 옵티팜 관계자는 “돼지췌도이식 전임상 및 임상시험에 쓰일 고품질의 DPF 원료동물을 확보하기 위해 기존 DPF 시설을 새로 짓고 있다”며 “12월말 리모델링을 마치면 시운전을 거쳐 내년부터 본격가동할 예정”이라고 말했다. 옵티팜은 현재 내년 중순께 돼지췌도이식 전임상 진입을 목표로 지난 5월부터 영장류 대상 비임상 파일럿 테스트를 진행 중이다.
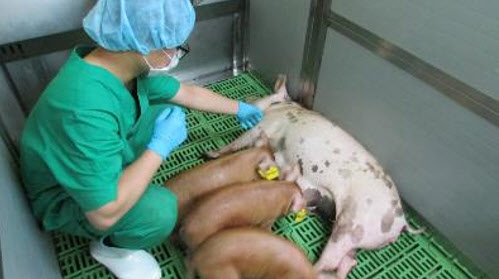 | | 옵티팜 연구원이 메디피그를 돌보는 모습(사진=옵티팜) |
|
원균제어시설(DPF·Designated Pathogen Free)이란 외부로부터 들어오는 병원균을 차단하는 완벽한 공조제어 시스템이 갖춰진 곳이다. 이 시설에서 태어나 유지·관리한 돼지를 DPF 돼지라고 한다. 이종이식에 활용할 돼지들이기 때문에 실험용 미니피그보다 훨씬 까다로운 기준의 시설에서 태어나고 자라야 한다. 아직 국내외에서 DPF 돼지에 대한 명확한 기준은 만들어지지 않았지만 세계이종장기학회 가이드라인은 146개의 세균, 바이러스, 곰팡이 등이 시설과 돼지에서 없어야 한다고 권고하고 있다.
현재 옵티팜은 기존 DPF시설을 통해 연간 100두의 DPF돼지를 보유·관리하고 있다. 이번 공사로 당장 DPF돼지의 두수가 늘어나지는 않는다. 다만 기존 특성균부재(SPF)시설과 DPF사이 수준이던 시설의 청정도를 세계이종장기학회의 DPF 가이드라인 수준으로 높이는 것이 목표다.
현재 이종장기이식과 관련된 임상시험을 준비하는 기업은
제넨바이오(072520)와 옵티팜 두 곳이다. 제넨바이오는 일찌감치 전임상을 마치고 현재 식약처에 이종췌도이식 1상 임상시험계획(IND)을 신청, 옵티팜보다 임상단계가 앞서있다.
이번이 세 번째 IND 신청인 제넨바이오는 앞서 돼지 종류에 따라 태어날 때부터 보유하고 있는 돼지내인성레트로바이러스(PERV) 감염원 안전성 확보 등을 우려하는 중앙약사심의위원회(중앙약심)으로부터 임상진입 재검토 의견을 받고 IND를 철회한 바 있다. 사실상 중앙약심은 이종장기학회가 언급한 146개 바이러스가 제넨바이오가 임상에 사용하는 무균돼지에서 나오지 않는다는 것을 입증할 자료를 제넨바이오에 요구한 것이다. 이후 자료를 보완해 IND 철회 사흘만에 재신청한 제넨바이오는 다시 식약처의 IND 승인을 기다리는 상태다. 하지만 승인 가능성에 대해서는 업계에서도 의견이 분분하다. 올해 이종장기이식에 대한 중앙약심의 입장이 다소 전향적으로 바뀌었지만 잠재 바이러스에 대한 우려는 여전하며 제넨바이오가 당장 이 같은 우려를 해소할 뾰족한 수가 없다는 이유에서다.
옵티팜측은 이번 생산시설 신축으로 향후 전임상 및 임상 진행시 PERV 감염원에 대한 식약처의 우려를 덜어낼 수 있을 것으로 기대하고 있다. 업계에 따르면 식약처는 옵티팜, 제넨바이오를 포함한 주요 관련 기업들과 이종이식 제제 관련 논의를 진행하고 있고 연말께 가이드라인을 확정해 발표할 예정이다.
올 초 미국 메릴랜드대 연구진이 돼지 심장을 사람에 이식하는 데 성공하자 옵티팜 등 관련 기업의 주가가 오르는 등 관심을 받았다. 하지만 국내엔 이종장기이식에 대한 가이드라인이 명확하지 않아 연구개발에 있어 막다른 길에 놓인 상태다. 미국 식품의약국(FDA)는 이종이식 임상 필요성에 동의하며 이를 위한 지침을 논의 중이다.




![美 AACR 약발은 하루뿐?…긍정적 데이터에도 투심 부진[바이오 맥짚기]](https://image.edaily.co.kr/images/Photo/files/NP/S/2026/04/PS26042300579b.jpg)


!['불성실공시 제재' 촉발한 삼천당 ‘97억 매출’…캐나다 처방액 38억 불과[only 이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042400548b.jpg)