팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 석지헌 기자] 정부가 이르면 내년 1월 말부터 코로나19 백신과 치료제 개발사들을 대상으로 대대적인 사업 적절성 점검에 나선다. 올해 말 코로나19 백신 ·치료제 신약개발사업단이 운영을 종료하면, 외부 용역을 통해 사업단의 지원 과제 선정 과정과 선정된 기업들의 개발 현황 등을 면밀히 살펴볼 방침이다. 개발 중단 선언을 한 업체들 외에도 임상시험에 좀처럼 속도를 내지 못하고 있는 업체들까지도 검사 대상에 포함될 전망이다.
27일 제약·바이오 업계에 따르면 보건복지부는 이르면 내년 1월 말부터 임상지원 사업을 통해 코로나19 백신·치료제 개발에 나섰던 제약·바이오 기업을 대상으로 사업 전반에 대한 적절성을 검토하는 평가 용역을 진행한다. 그 동안 정부의 ‘코로나 백신 및 치료제 임상지원 사업’을 통해 지원 받은 기업은 총 14곳이다.
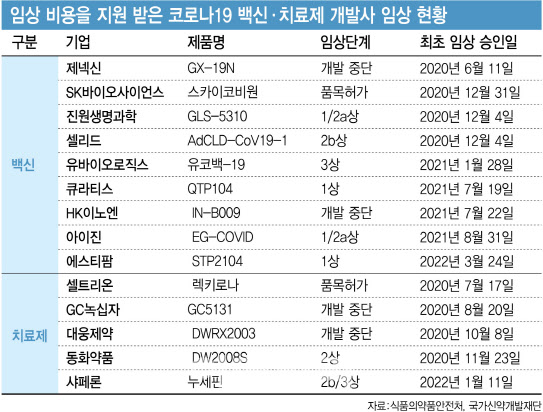 | | [이데일리 김정훈 기자] |
|
백신은
진원생명과학(011000) 셀리드(299660) 유바이오로직스(206650) 큐라티스
HK이노엔(195940) 아이진(185490) 에스티팜(237690) 제넥신(095700) SK바이오사이언스(302440) 9개 기업이고 치료제는
셀트리온(068270) 녹십자(006280) 대웅제약(069620) 동화약품(000020) 샤페론(378800) 5개 기업이다. 이들 기업은 정부로부터 총 1679억원에 달하는 국가 연구비를 지원 받았지만 신약 개발에 성공한 사례는 셀트리온과 SK바이오사이언스 뿐이다. 이 중 녹십자, 대웅제약, 제넥신, HK이노엔이 개발 중단을 선언했다. 녹십자는 이번 국정감사에서 정부 개발 지원비 58억원을 받은 후 임상 초기 단계에서 개발 중단을 선언해 지원비 ‘먹튀’ 논란이 일기도 했다.
내년 평가에는 이번에 논란이 된 녹십자 뿐 아니라 임상 비용 지원을 받은 업체들 대다수가 줄줄이 도마위에 오른다. 임상 개발 중단을 발표한 기업 뿐 아니라 임상을 진행 중이지만 지나치게 연구가 지연되고 있거나 주가 조작 의혹 등이 의심되는 기업까지 포함되는 것이다. 평가 결과, 문제가 있다고 밝혀지는 기업들의 경우 연구비를 전액 환수하거나 사안 경중에 따라 3~5년까지 앞으로 정부 연구개발사업에 참여하기 어려워질 수 있다.
복지부 관계자는 “문제가 되는 곳에 대한 기준을 잘 잡을 계획이다. 끝까지 개발을 안 하고 중단된 기업도 대상이 되겠지만, 임상 진행 상황에서도 지나치게 지연되는 곳도 살펴볼 것”이라며 “행정 절차상으로 걸러내기 어려운 부분이 있어 경찰수사가 필요할 수도 있다. 일단은 근거를 두고 있는 법률에 따라 할 수 있는 부분이 어디까지인지 제대로 점검해 볼 것”이라고 말했다.
실제 개발비 지원을 받은 업체들 중 상당 수가 임상에 난항을 겪는 것으로 분석된다.
진원생명과학은 GLS-5310 백신에 대해 2020년 12월 4일 임상1/2a상을 승인받은 후 2년 가까이 돼 가도록 뚜렷한 성과를 내지 못하고 있다. 진원생명과학이 지난해 11월 23일 공시한 투자설명서를 보면 GLS-5310의 부스터샷을 위한 DNA 백신 임상3상 개발과 승인을 올해 1분기로 예상하고 있다. 백신 허가는 올해 4분기로 명시한 바 있다. 하지만 아직까지 한국 임상 기준 1/2a상 단계에 머물러 있는 상황이다.
진원생명과학은 경구용 코로나19 치료제 ‘GLS-1027’도 개발 중이다. 이 파이프라인은 정부 지원을 받지는 않았다. 지난해 9월 국내 2상 임상시험계획을 승인받은 후 1년 지났지만 여전히 임상2상 단계다. 투자설명서를 보면 이 역시 임상3상 연구 승인 획득을 올해 1분기, 품목허가는 올해 3분기로 각각 목표한 바 있다. 진원생명과학은 코로나19 백신과 치료제 개발 이슈로 시장 주목을 받았다. 2020년 3월27일 ‘2020년도 질병관리본부 용역과제인 ‘코로나19 백신후보물질 개발 사업’에 우선 순위 협상대상자로 선정되면서 7640원이던 주가는 일주일 만에 1만5100원(2020년 4월 7일 종가 기준)까지 약 97% 상승하기도 했다.
셀리드는 2020년 12월부터 백신 개발에 뛰어들었고 2021년과 2022년 두 차례 임상 개발비 지원을 받았으나 개발 과정에서 임상시험계획서 변경, 오미크론 변이 대응 백신 파이프라인 추가 등으로 아직 임상2b상 단계에 머물러 있다. 동화약품은 천연물 코로나19 치료제 후보물질 ‘DW2008S’에 대해 2020년 11월 23일 첫 임상 승인을 받은 후 2년이 돼 가지만, 의약품안전나라에 따르면 아직도 임상 환자 ‘모집중’이다.
에스티팜과 아이진, 큐라티스 등 3곳은 mRNA 코로나19 백신 임상을 진행 중이다. 아이진은 국내와 호주에서 임상1상 투여 완료 후 중간결과 분석을 진행 중이다. 에스티팜은 올해 3월 임상1상 허가를 받았지만 임상시험계획 승인 후 8개월 가량이 지나도록 아직 환자 모집 단계에 진입하지 못했다. 지난해 7월 19일 임상1상을 승인받은 큐라티스는 1년 3개월 가량 지난 현재 임상1상 대상자 모집 및 투약 후 결과 분석과 추적 관찰 단계에 있다.
전문가들 사이에서는 팬데믹 종식이 가까워지고 있는 만큼 환자 수나 임상 계획 수정등을 심각해 고려해야 할 시점이라는 지적이 나온다.
한 임상시험 디자인 전문가는 “표준은 없지만 1년이상 지연은 중대한 또는 의미있는 지연으로 여겨질 것”이라며 “조기 종료를 선언하거나 환자 수를 조정하는 등 결단을 내려야 하는 시기”라고 말했다.






![고영, 어닝서프라이즈에 '上'…바이젠셀·툴젠도 상승세[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042700146b.jpg)


![일라이 릴리 10조 베팅·영국 의료 정보 유출[클릭, 글로벌 제약·바이오]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042601061b.jpg)