팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 송영두 기자] 국내 바이오 1호 유니콘 기업 에이프로젠의 주력 사업이 아직 본궤도에 오르지 못하고 있는 것으로 나타났다. 레미케이드 바이오시밀러를 상용화했지만 2년째 해외 매출이 전무하다.
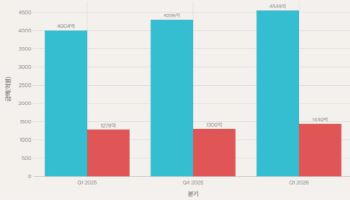
21일 금융감독원 전자공시시스템에 따르면 에이프로젠은 지난해 3분기까지 매출액 약 205억원, 영업손실 약 691억원을 각각 기록했다. 매출은 전년 같은기간 194억원 대비 약 5% 증가했지만, 영업손실은 최근 3년 동안 급격히 확대되고 있다. 2019년 약 399억원이던 영업손실은 2020년 약 712억원으로 증가했고, 지난해에는 3분기만에 영업손실이 전년 수준에 근접한 상태다. 주력 사업인 바이오시밀러 부진이 실적 하락 원인으로 꼽힌다.
에이프로젠은 약 2년 전 유니콘 기업으로 등극하면서 유명세를 치렀다. 지난 2019년 12월 글로벌 시장조사업체 CB인사이트에 국내 11번째 유니콘 기업으로 등재됐다. 특히 바이오 1호 유니콘 기업이 되면서 업계 반향을 일으켰다. 유니콘 기업은 기업가치가 10억 달러(약 1조원) 이상인 스타트업 기업이다. 에이프로젠과 같이 유니콘 기업으로 등재된 쿠팡과
크래프톤(259960)은 각각 미국 나스닥, 한국 코스피 시장에 상장되면서 유니콘기업의 기대치를 높이고 있다.
 | | 에이프로젠 매출 실적.(자료=에이프로젠 2021년 3분기 보고서) |
|
레미케이드 바이오시밀러, 2년째 매출 0원 바이오 1호 유니콘 기업인 에이프로젠 상황은 녹록치 않다. 바이오시밀러 사업을 영위하는 에이프로젠은 지난 2017년 레미케이드 바이오시밀러를 개발해 상용화했다. 일본 니찌이꼬제약과 판매계약을 맺고 그해 11월부터 일본 시장에서 판매됐다. 2018년 329억원의 매출을 올렸으나 2019년 매출은 50억원으로 감소했다.
특히 문제는 레미케이드 바이오시밀러가 에이프로젠이 유일하게 개발한 제품이고, 유일한 매출처인 일본에서 2년 연속 매출을 발생시키지 못하고 있다는 점이다. 에이프로젠의 지난해 3분기 보고서에 따르면 2020년과 2021년 3분기까지 레미케이드 매출은 0원이다. 기타제품으로만 약 200억원 수준의 매출을 기록하고 있다.
에이프로젠 관계자는 “레미케이드 바이오시밀러 일본 판매의 경우 니찌이꼬제약이 담당해 정확한 수치는 알 수 없지만, 판매가 늘고 있는 것으로 확인했다”며 “2년째 매출이 없는 것은 니찌이꼬제약에 아직 재고가 남아있어 추가 물량 공급이 이뤄지지 않았기 때문이다. 기타제품 매출은 미국에서 품목허가를 진행하기 위한 임상시험용 의약품 생산 등에 따른 것”이라고 말했다.
 | | 에이프로젠 오송공장.(사진=에이프로젠) |
|
터키 진출 약 4년째 공회전, 美 진출도 1년+α 에이프로젠은 2018년부터 유럽시장 진출을 꾀하고 있지만 큰 진척이 없는 상태다. 2018년 4월 터키 보건당국에 레미케이드 바이오시밀러 제품 품목허가를 신청했지만 약 4년이 흐른 지금까지도 여부가 결정되지 않은 상황이다. 에이프로젠은 2011년 11월 바이넥스와 위탁생산 계약을 체결해 레미케이드 바이오시밀러 제품은 바이넥스 공장에서 생산된다. 터키에서 품목허가가 승인되면 바이넥스는 제품을 직접 터키 압디사에 공급할 예정이었다. 바이넥스 관계자는 “2018년 4월 에이프로젠 바이오시밀러 제품에 대해 터키에 품목허가를 신청한 것이 맞다”며 “관련 업무는 우리가 진행하고 있다. 하지만 2020년 코로나19가 발생하면서 관련 작업이 지연되고 있다”고 말했다.
당초 회사 측이 올해로 예상했던 미국 품목허가 신청도 1년 이상의 시간이 소요될 것으로 예상된다. 에이프로젠은 2019년 레미케이드 바이오시밀러 미국 임상 3상을 완료했다. 미국 식품의약국(FDA) 품목허가를 신청하기 위해 충북 오송에 연면적 약 5만2247㎡(1만5000평) 규모, 연간 24만 리터 의약품 생산이 가능한 생산시설을 완공한 상태다. 여기에는 약 3700억원이 투입됐다. 현재 미국 FDA 실사를 준비 중인 것으로 알려졌다.
회사 관계자는 “미국 시장에 진출할 레미케이드 바이오시밀러는 오송공장에서 생산될 예정이다. FDA 품목허가를 획득하려면 생산시설에 대한 실사가 진행된다”며 “임상은 바이넥스 생산 의약품으로 했기 때문에 오송공장에서 생산한 제품과 동등성을 입증해야 해 그런 부분들을 준비 중이다. 품목허가 신청은 내년으로 예상한다”고 말했다. 이 외 허셉틴 바이오시밀러는 2019년 5월 미국 임상 1상을 완료했고, 글로벌 임상 3상을 준비 중이다. 리툭산 바이오시밀러는 전임상을 완료하고 글로벌 임상 1상 및 3상을 계획하고 있다.
회사 측은 코로나 사태로 인해 터키와 미국 진출 시기가 지연됐지만, 시장 진출 시 원가 경쟁력을 통해 승산이 있을 것으로 내다보고 있다. 에이프로젠 관계자는 “실적 악화는 예상했던 규모로 큰 문제가 없을 것으로 판단하고 있다. 회사는 비용이 적게 드는 작은 배양기로 경쟁 바이오시밀러 기업 등과 유사한 규모의 의약품을 생산할 수 있어 원가 경쟁력을 실현했다”며 “바이오시밀러 제품이 미국과 유럽 시장에 진출하면 에이프로젠이 가지고 있는 원가 경쟁력을 통해 충분히 승산이 있을 것으로 기대하고 있다”고 말했다.




![로킷헬스케어 1.9조 수주 계약이라더니…구속력 無·매출 전환율 0.8%[only 이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/05/PS26050400118b.jpg)
!["516억 조달로도 임상 1상 자금 부족"...로킷아메리카, 공모 흥행 우려도[only 이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/05/PS26050800010b.jpg)

