[이데일리 송영두 기자] 올해 세계 최초 타이틀을 가지는 다양한 세포유전자치료제가 허가를 받을 것으로 예측됐다.
19일 한국바이오협회 ‘2023년 글로벌 세포유전자치료제 시장 동향’ 리포트에 따르면 세계 최초로 유전자가위 크리스퍼(CRISPR) 기술을 활용한 유전자치료제가 허가 받을 것으로 전망된다.
미국 크리스퍼 테라퓨틱스와 미국 버텍스 파마슈티컬스가 공동 개발한 크리스퍼 유전자 편집 치료제 ‘엑사셀(exa-cel)이 미국 식품의약국(FDA)에 품목허가를 신청할 계획이다. 크리스퍼 유전자 가위는 DNA를 찾아내고 편집이 가능한 RNA와 Cas9으로 이뤄진 것으로, 유전자를 가위로 자르듯 잘라내고 편집해 치료하는 기술이다. 이 외에도 세계 최초 고형암에 대한 적응세포치료제와 세계 최초 뒤센느 근이영양증 유전차 치료제도 허가를 받을 것으로 관측된다.
세포유전자치료제 분야는 지난해 투자액이 사상 처음으로 감소했지만, 관련 연구는 여전히 활발하게 이뤄지고 있는 것으로 나타났다.
2022년 한해동안 세계 세포유전자치료제 기업에 대한 투자액은 126억 달러로, 이는 2021년 227억 달러 대비 44% 감소한 수치다. 세계 세포유전자치료제 투자는 2019년 98억 달러, 2020년 199억 달러로 지속 증가 추세에 있었다.
투자는 감소했지만, 지난해 미국과 유럽에서 세포유전자치료제 6개가 허가를 받았고, 5개가 새로운 지역 또는 새로운 적응증으로 허가되는 큰 성과를 나타냈다. △얀센과 레전드 바이오텍이 공동개발한 카빅티(CAR-T) △바이오마린 파마슈티컬 록타비안(유전자치료제) △PTC 테라퓨틱스 업스타자(유전자치료제) △유니큐어와 CLS베링이 공동개발한 헴제닉스(유전자치료제) △페링제약 애드스틸라드린(유전자치료제) △아타라 바이오테라퓨틱스 엡발로(세포치료제)가 주인공이다.
또한 5개의 세포유전자치료제는 새로운 지역과 새로운 적응증으로 허가돼 주목받았다. △BMS 브레얀지(CAR-T) △노바티스 킴리아(CAR-T) △카이트 파마 예스카타(CAR-T) △블루버드 바이오 진테글로(유전자치료제)와 스카이소나(유전자치료제) 등이다.
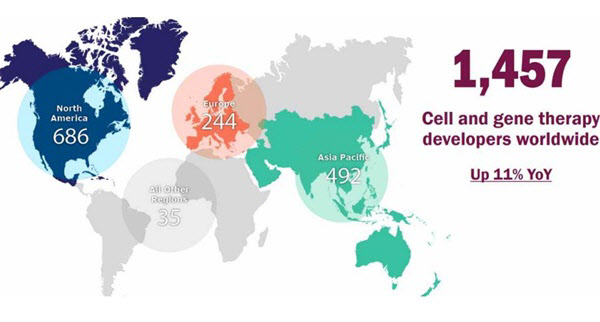 | | 세포유전자키료제 개발 기업 분포도.(자료=한국바이오협회) |
|
현재 세포유전자치료제를 개발하고 있는 기업은 1457개다. 이는 지난해 대비 11% 증가한 수치다. 이중 686개사(47.1%)는 북미 지역에 위치해있고, 492개사는 아시아태평양 지역에, 224개사는 유럽에 분포해있다. 기타 지역은 35개사로 집계됐다.
이들 기업이 진행 중인 세포유전자치료제 임상은 2220개에 달한다. 지역별로는 북미지역 43%, 아시아태평양 38%, 유럽 18% 순이다. 특히 지난해 254개의 관련 임상이 추가됐는데, 이중 48%는 아시아태평양 지역에서 새롭게 시작됐다.
202개의 임상 3상이 진행 중에 있으며, 유전자편집기술을 통한 임상시험도 100개 이상이 진행 중이다. 특히 진행중인 모든 임상의 60%가 종양을 타깃하고 있고, 고형암과 혈액암의 비중이 50%로 비슷했다.
임상 개발이 가장 활발하게 이뤄지는 지역은 미국으로 나타났다. 미국에서는 올해 최대 14개 세포유전자치료제 허가 여부가 결정되고, 최소 5개 이상이 허가를 받을 것으로 예상된다. 이에 발맞춰 미국 FDA도 세포유전자치료제에 대한 심사역량과 전문성을 확보하기 위해 담당부서를 확대 개편한다. 현재 300명인 심사인력을 향후 5년동안 400명 규모로 늘릴 계획이다.
한편 세포유전자치료제 분야에서 리더러 평가받던 유럽은 첨단바이오의약품으로 허가받은 24개 치료제 중 7개가 보험 급여 등의 이슈로 철수했다. 지난해 신규로 추가된 임상연구도 단 3개에 불과했다.



![[임상 업데이트] LG화학, 경구용 희귀비만 신약 2상서 체중 감소 효과](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200105b.jpg)



![인투셀, 특허이슈에 장외 하한가…퓨쳐켐, 진단제 국내 품목허가 추진[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071000247b.jpg)

