[이데일리 김명선 기자] 올해 미국과 유럽 시장에 진출할 기회를 얻은 국산 의약품이 대부분
셀트리온(068270)과 삼성바이오에피스의 바이오시밀러로 나타났다. 양사는 자가면역질환, 황반변성 외에 대장암과 골다공증 등 다양한 질환에서 글로벌 경쟁을 예고했다.
 | | (사진=셀트리온 홈페이지) |
|
3일 제약·바이오 업계에 따르면 올해 미국 식품의약국(FDA)과 유럽의약품청(EMA)에서 판매 승인받은 국내 개발 의약품은 지금까지 4개로 추산된다. 통상 EMA 산하 약물사용자문위원회(CHMP)가 긍정 의견을 내면 2~3개월 후 판매 허가로 이어져 사실상 판매 허가로 간주하는 점도 고려해서다.
지난 1월 EMA 승인 권고를 획득한
SK바이오팜(326030)의 케미칼 신약 ‘엑스코프리(성분명 세노바메이트)’를 제외하면 나머지는 삼성바이오에피스와 셀트리온 제품이다. 셀트리온의 코로나19 치료제 ‘렉키로나주’는 바이오 신약으로 나머지 제품은 모두 바이오시밀러다.
올해 삼성바이오에피스는 제넨텍 황반변성치료제 ‘루센티스(성분명 라니비주맙)’를 복제한 바이오시밀러 ‘바이우비즈(프로젝트명 SB11)’에 대해 미국과 유럽에서 모두 판매 허가를 받았다. 삼성바이오에피스는 이 허가로 4조원 규모의 라니비주맙 시장으로 사업 영역을 확대했다.
셀트리온과 삼성바이오에피스는 또 모두 9조원에 달하는 ‘아일리아(애플리버셉트)’ 시장을 노리고 바이오시밀러 글로벌 임상 3상도 진행 중이다. 이번 바이우비즈 허가로 황반변성치료제 바이오시밀러 시장에서는 삼성바이오에피스가 셀트리온에 한 발 앞서게 됐다.
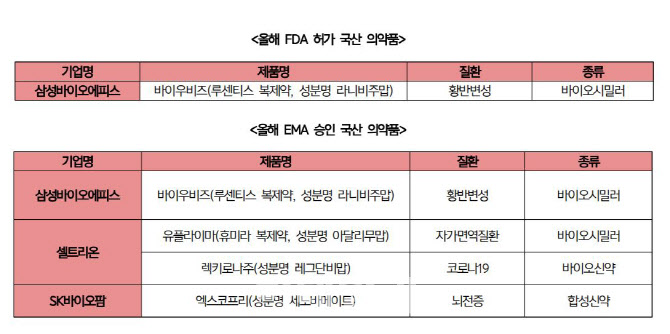 | | 올해 FDA와 EMA로부터 승인 받은 국산 의약품. |
|
셀트리온은 애브비가 개발한 자가면역질환 치료제 ‘휴미라(아달리무맙)’의 바이오시밀러인 ‘유플라이마(CT-P17)’에 대한 EMA 판매 승인을 2월 받았다. 지난해 기준 연간 22조원 시장이다. 지난해 11월 셀트리온은 FDA에도 유플라이마 허가를 신청해 승인을 기다리는 상황이다.
이미 삼성바이오에피스는 휴미라에 대한 바이오시밀러를 미국과 유럽에서 허가받은 바 있어 정면 경쟁이 펼쳐지게 됐다. 유플라이마 허가로 삼성바이오에피스와 셀트리온이 해외 시장에 내놓게 된 자가면역질환 바이오시밀러도 3종으로 같아졌다.
글로벌 자가면역질환 시장에서 두 기업은 존슨앤드존슨 ‘레미케이드(인플릭시맙)’ 시장을 두고도 경쟁을 펼치고 있다. 삼성바이오에피스는 ‘렌플렉시스(SB2)’를 2016년과 2017년 유럽과 미국에서 허가받고 판매 중이고 셀트리온은 ‘램시마’를 미국과 유럽에서 출시했다.
레미케이드 시장 점유율은 셀트리온이 다소 앞선다. 올해 3분기 기준 램시마의 유럽 시장 점유율은 53%로 24.5%를 기록한 레미케이드를 뛰어넘었다. 미국 시장 점유율은 레미케이드가 67.3%, 램시마가 21.2%다. 렌플렉시스는 7%다.
글로벌 자가면역질환 시장을 둘러싼 삼성바이오에피스와 셀트리온의 정면 승부도 예고된다. 현재 삼성바이오에피스와 셀트리온 두 기업 모두 얀센의 ‘스텔라라(우스테키누맙)’ 바이오시밀러 임상3상 진행 중이다. 지난해 기준 이 시장 규모는 약 8조원이다.
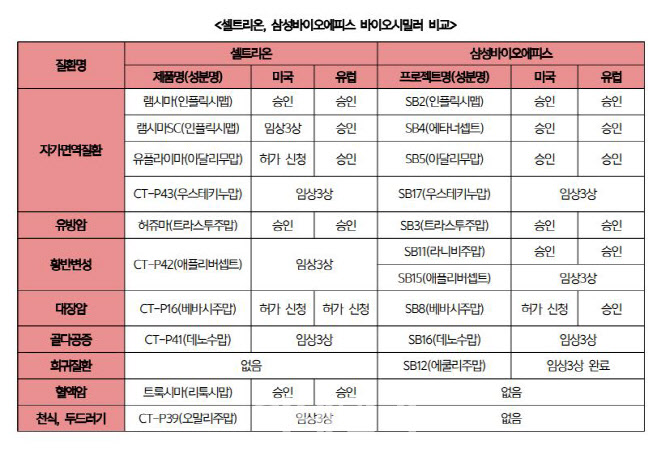 | | 셀트리온과 삼성바이오에피스가 글로벌 임상을 진행 중이거나 미국과 유럽에서 개발하고 있는 바이오시밀러 현황. |
|
두 기업은 앞으로 대장암, 골다공증 시장에서도 맞대결을 예고했다. 삼성바이오에피스는 로슈 종양질환 치료제 ‘아바스틴(베바시주맙)’의 바이오시밀러 ‘에이빈시오(SB8)’를 유럽에서 이미 허가받았고 FDA에는 2019년 11월 허가를 신청했다. 셀트리온도 아바스틴 바이오시밀러 ‘CT-P16’에 대해 미국과 유럽에 허가를 신청한 상태다. 지난해 기준 아바스틴 글로벌 시장 규모는 약7조7000억원이다.
골다공증 시장에서도 삼성바이오에피스와 셀트리온 모두 암젠이 개발한 ‘프롤리아(데노수맙)’에 대한 글로벌 임상3상에 착수한 상태다.
셀트리온 관계자는 “최초로 항체 바이오시밀러를 상업화한 만큼 추가 파이프라인에 대한 임상 및 허가를 빠르고 합리적으로 진행할 수 있다”고 자신했다. 삼성바이오에피스 관계자는 “사업 포트폴리오가 안과질환, 희귀질환 등 다양하다”라며 “유럽에서 휴미라, 엔브렐, 레미케이드 바이오시밀러로 시장을 리딩하며 데이터 경쟁력을 확보하고 있다”고 밝혔다.








![美FDA 허가 두고 줄기세포치료제 개발사 희비교차…메디포스트 하락·코아스템 상승[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25070300200b.jpg)

