팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김유림 기자]
한미약품(128940)의 핵심 파이프라인 포지오티닙이 결국 미국식품의약국(FDA) 산하 항암제자문위원회(Oncology Drug Advisory Committee, ODAC)로부터 신속승인 반대 의견을 받았다. 전문가들은 오히려 악재해소로 봤으며, 11월 말 FDA 최종 심사 전까지 하락은 더 이상 없을 것으로 전망했다. 특히 포지오티닙의 밸류에이션 대비 과도한 주가 하락이라고 평가했다.
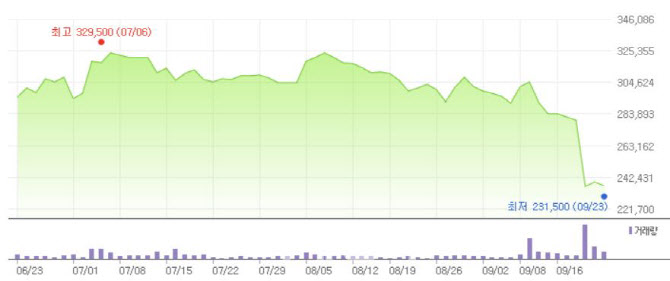 | | 최근 3개월 한미약품 주가 추이. (자료=네이버금융) |
|
23일 마켓포인트에 따르면 한미약품의 주가는 지난 21일 하루 만에 전 거래일 대비 15.54%(4만3500원)가 급락했다. 시가총액은 약 5400억원이 증발하면서 3조원대가 무너졌다. 시총이 2조원대로 내려앉은 건 지난 2020년 1월 17일 이후 처음이다.
한미약품의 주가 급락의 이유는 ‘포지오티닙’ 악재 단 한가지다. ODAC에서 포지오티닙에 대한 부정적인 의견을 담은 브리핑 문서를 발표한 여파다. ODAC는 기존 치료제와 비교해 유용성이 크지 않고 안전성도 문제가 있다고 판단했다. 이날 결국 표대결에서 신속승인 반대 9표, 찬성 4표로 결론이 나왔다. ODAC 위원들은 포지오티닙이 환자에게 주는 혜택(benefit)보다 위험(risk)이 더 크다고 의견을 낸 것이다.
반면 시장과 업계에서는 악재해소로 판단했다. 한 증권사 바이오 연구원은 “이미 21일 급락으로 모든 악재는 다 반영됐다고 보면 된다. ODAC 결론에 대한 불확실성까지 없어지면서 다시 주가는 반등할 것”이라며 “다만 대내외 매크로 악재가 너무 심해서 기존에 빠진 주가가 빠른 속도로 올라가긴 힘들고, 점차 오를 것으로 예상한다”고 관측했다.
한미약품의 밸류에이션에 포지노티닙이 극히 적은 비중을 차지했으며, 과도한 주가 하락이라는 분석도 나온다. 또다른 증권사 바이오 연구원은 “지금 포지오티닙 개발 자체가 실패한 게 아니다”면서 “포지오티닙 밸류에이션 전체를 넘어선 주가 하락은 과했다. 국내 주식시장의 센티멘털 문제가 더 크게 반영된 것 같다”고 분석했다.
실제로 ODAC 발표 전에 발간된 국내 주요 증권사에서 작성한 한미약품 리포트를 살펴보면 포지오티닙이 차지한 밸류에이션은 하나금융투자 1100억원, 유진투자증권 1200억원, 삼성증권 2390억원, 현대차증권 3429억원 등 1100억~3400억원에 불과하다.
키움증권은 한미약품의 목표주가에 포지오티닙 신약 가치를 포함조차 하지 않았다. 허혜민 키움증권 연구원은 “2023년 로열티 유입 또한 25억원에서 2026년 106억원으로 전망돼 포지오티닙에 대한 기대감이 높지 않았다. 목표주가에 포지오티닙 신약 가치를 포함하지 않았다”며 “한미약품의 내년 PER은 31배로 밸류에이션 매력도 높아진다. 3분기 양호한 실적과 ‘내년 상반기 트리플 어고니스트 NASH 임상 2b상 중간 데이터도 발표 예정이다”고 했다.
포지오티닙은 한미약품이 2012년 미국 기업 스펙트럼사에게 글로벌 판권을 이전한 비소세포폐암 치료제다. EGFR 억제 기전, HER2 변이를 타깃으로 한다. 스펙트럼은 올해 2월 15일 임상 2상인 ZENITH 20의 코호트2 데이터에 근거해 FDA에 신속승인 심사를 신청했다.
ODAC은 암 치료에 사용하기 위한 시판 및 임상 제품의 유효성과 안전성에 관한 데이터를 검토하고 평가하는 전문가들로 구성된 독립위원회다. 위원회는 FDA에 적절한 권고안을 제시하지만, 이 권고안은 구속력이 없으며 제품 승인은 FDA가 최종 결정한다. 2009~2022년 ODAC과 FDA의 의견 불일치 비율은 약 10%정도다. 포지오티닙 FDA 신속승인 최종 결정은 11월 24일까지 남았다.
한미약품 관계자는 “임상 3상을 끝낸 약물에 대한 ODAC의 결론이 아니고, 신속승인 심사에 대한 의견일 뿐이다. 포지오티닙이 갖고 있는 가치에 비해서 당사의 주가가 너무 과하게 빠진 측면이 있다고 생각한다”며 “ODAC 의견이 뒤집힌 사례도 있기 때문에 FDA의 결정이 나오는 11월 24일까지는 좀 더 지켜봐야 할 거 같다”고 말했다.