팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김진호 기자] 미국 바이오젠과 일본 에자이가 합작한 치매치료제 신약 후보물질 ‘레카네맙’(개발 코드명 BAN2401)의 확증 3상 결과 발표를 두고 논란이 일고 있다. 효과가 뚜렷하지 않은데다 이와 관련한 사망 사례가 포함되면서다.
바이오젠은 지난해 세계 최초의 치매치료제 ‘아두헬름’(성분명 아두카누맙)을 미국에서 출시했다가 부작용 문제로 진통을 겪었다. 업계에서는 치매 정복을 향한 바이오젠 재도전에 대한 성공 가능성이 거론되고 있다.
 | | (제공=픽사베이) |
|
지난달 29일(현지시간) 바이오젠과 에자이 등은 레카네맙에 대한 글로벌 임상 3상 세부 결과를 공표했다. 레카네맙은 치매의 일종인 알츠하이머의 주된 원인 물질로 알려진 ‘아밀로이드베타’(Aβ)를 타깃하는 항체다. 양사는 이번 발표에서 “1차 평가 지표로 설정한 ‘치매임상평가척도총합’(CDR-SB)을 초과 달성했다”고 평가했다.
양사에 따르면 북아메리카, 유럽, 아시아 등 235개 지역에서 레카네맙 투여군(898명)과 위약 대조군(897명) 등 총 1795명의 알츠하이머 환자를 대상으로 확증 임상 3상이 진행됐다. 이들에게 격주로 레카네맙과 위약을 정맥주사했고, 1치 평가 종점인 18개월 시점에서 CDR-SB과 함께 2차 평가 지표인 ‘아밀로이드 양전자 단층촬영(PET)값’ 등을 비교분석했다.
그 결과 양사는 “레카네맙 투여군에서 CDR-SB은 평균 1.21, 위약군은 1.66의 값을 얻었다”며 “전반적으로 인지 및 기능 척도에서 0.45만큼 낮춘 것은 통계적으로 매우 유의미한 결과를 얻었다”고 밝혔다. 레카네맙을 투여한 알츠하이머 환자들의 인지 기능 저하 속도가 대조군 대비 27% 느려질 수 있다는 설명이다.
이에 더해 18개월 뒤 아밀로이드 PET값의 평균 변화율 역시 레카네맙 투여군은 -55.6점, 위약군은 3.6점으로 나타났다. 바이오젠과 에자이 측은 이같은 결과를 두고 뇌 속 아밀로이드베타 플라크(덩어리)로 인한 부담이 크게 감소한 것으로 분석했다.
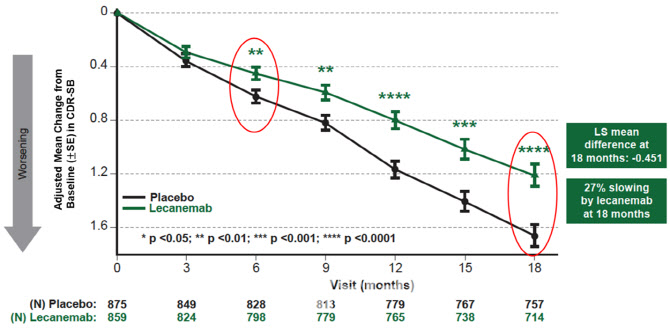 | | 미국 바이오젠과 일본 에자이가 공동 개발한 알츠하이머 신약 후보물질 ‘레카네맙’의 확증 임상 3상 결과, 1차 지표인 ‘치매임상평가척도총합’(CDR-SB)를 통계적으로 유의미하게 개선했다. 레카네맙을 투여군의 CDR-SB는 평균 1.21로 위약군(1.65)보다 낮았으며, 이는 인지 저하 속도를 약 27% 늦추는 것으로 해석됐다.(제공=바이오젠) |
|
하지만 이런 레카네맙의 효능 미비 및 부작용 가능성 등 두 가지에 대한 우려가 나오고 있다. 우선 1차 평가 지표인 CDR-SB로 인한 환자의 ‘인지 기능 개선’ 효과가 비교적 뚜렷하지 않다는 점이다.
국내 신약개발 업계 한 대표는 “보통 항암제나 백신 등 신약을 개발할 때 초기 임상을 통한 효능 평가에서 기존 치료제나 위약군 대비 30% 이상 개선되는 효과가 관찰돼야만 추가 개발을 진행하는데 큰 동력으로 얻게 된다”며 “이번 결과에서 1차 지표에 대한 개선 정도가 27% 하는 것은 효과가 크게 높지 않은 것”이라고 운을 뗐다.
사실상 투여군과 위약군 사이에 CDR-SB값의 차이가 현재(0.45) 대비 2~4배 이상 커져야 치료제로서 확실한 의미가 있다는 얘기다. 지난해 6월 FDA가 승인했던 ‘아두헬름’의 CDR-SB은 1.35이었으며, 당시에도 위약군(1.74) 대비 결정적인 차이가 관찰되지 않았었다. 그런데도 미국 정부의 퇴행성 뇌질환 신약 개발 독려 기조에 힘입어 아두헬름이 최종 품목 허가됐다.
그는 이어 “아두헬름은 승인 후 뇌부종 부작용으로 현장에서 힘을 잃었다. 이런 위험을 줄인 것을 보여준다면 1차 지표의 개선 정도를 떠나 레카네맙도 미국에서 승인될 수 있을 것으로 판단하는 것 같다”고 덧붙였다. 지난 7월 FDA는 레카네맙의 가속 승인 신청서를 수락해 심사를 진행하고 있다.
일반적으로 학계에서는 아밀로이드베타를 타깃하는 약물의 뇌부종(ARIA-E) 부작용을 경고하고 있다. 바이오젠과 에자이에 따르면 이번 확증 3상에서 레카네맙 투여군의 뇌부종 위험은 12.6%이며 위약(1.7%) 대비 약 7.4배 높은 것으로 나타났다. 대뇌 미세 및 거대 출혈 관련 부작용 역시 레카네맙 투여군(17.3%)이 위약군(9%)보다 약 2배 높았다.
반면 임상기간 사망자 수는 레카네맙 투여군(0.7%)과 위약군(0.8%)에서 비교적 엇비슷하게 나타났다. 지난 9월 80대 남성과 지난달 27일 65세 여성 등 두 명의 사망사례가 보고된 것이다.
바이오젠과 에자이 측은 과학 및 의학 전문 매체 사이언스를 통해 “심각한 뇌출혈로 2명이 사망했는데 이를 생검한 의사로부터 레카네맙 치료와 관련이 없는 것으로 판명됐다”고 밝힌 바 있다.
한편 이번 확증 임상 3상의 세부 결과에 대해 시장은 긍정적으로 받아들이고 있다. 나스닥에 상장된 바이오젠(BIIB)은 결과 발표 이튿날인 30일 시가 기준 309.73달러로 전날 종가(291.26달러) 대비 약 7% 상승했다.
글로벌 금융 웹사이트 ‘인베스팅닷컴’에 따르면 이날 기준 BIIB에 대해 애널리스트 32명 중 19명이 매수, 13명이 중립 의견을 제시하며, 바이오젠이 시장수익률을 초과할 것으로 내다보고 있다.







![지놈앤컴퍼니, 임상 본격화 기대감에 급등…숨고르기 들어간 바이젠셀[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26043000447b.jpg)


