팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김진호 기자] 미국 애브비가 크론병 관련 치료제 포트폴리오를 확장하는 데 주력하고 있다. 크론병에 널리 쓰던 애브비의 대표 약물, ‘휴미라’(성분명 아달리무맙)의 미국 내 물질 특허가 내년 초에 만료되기 때문이다.
최근 회사 측은 건선 치료제로 개발한 ‘스카이리치’(성분명 리산키주맙)의 적응증을 크론병으로 늘리는 데 성공했다.
셀트리온(068270), 독일 베링거인겔하임 등 국내외 개발사가 두루 완성한 휴미라 바이오시밀러가 시장에 진입하기 전에 애브비가 방어벽을 구축하고 있다는 평가가 나온다.
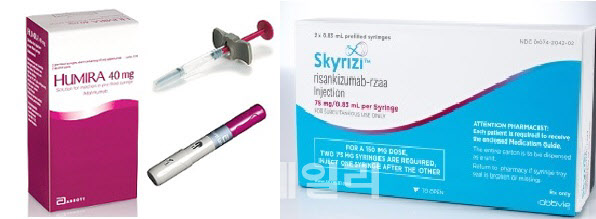 | | 미국 애브비의 자가면역질환치료제 ‘휴미라’(성분명 아달리무맙, 왼쪽)과 ‘스카이리치’(성분명 리산키주맙). (제공=애브비) |
|
최강자 ‘휴미라’ 특허 만료...“크론병 치료제 대안 필요해져” 22일 업계에 따르면 애브비가 가진 대표적인 자가면역질환 치료제는 크게 세 가지다. 염증 신호에 영향을 주는 종양괴사인자알파(TNF-α)를 억제하는 휴미라와 인터류킨(IL) 저해제인 스카이리치, 야누스 키나아제(JAK) 저해제 ‘린버크’(성분명 유파다시티닙) 등이 여기에 포함된다.
이중 가장 먼저 개발된 휴미라는 2000년대 중반 미국식품의약국(FDA)과 유럽의약품청(EMA)로부터 성인 크론병 1차 치료제로 품목 허가됐다. 이후 휴미라는 2012년 EMA와 2014년 FDA로부터 각각 6세 이상 소아 크론병 환자에게 사용할 수 있는 치료제로 적응증을 확대 승인받았다. 이 약물은 소아 크론병 환자가 쓸 수 있는 최초의 생물학적 제제로 이름을 올리면서 폭넓게 처방돼 왔다.
하지만 휴미라의 주요 물질 특허가 2014년 유럽을 시작으로 만료되기 시작했다. 가장 큰 시장인 미국에서 휴미라의 특허 기간이 연장됐지만, 이마저도 2023년 1월이면 모두 만료될 예정이다. 국내 삼성바이오에피스 ‘하드리마’와 셀트리온 ‘유플라이마’ 등을 포함해 내년 미국 출시를 앞둔 휴미라 바이오시밀러만 총 9종이다.
특히 지난해 10월 FDA는 베링거인겔하임이 개발한 ‘실테조’가 휴미라의 인터체인저블(대체 가능) 바이오시밀러로 평가된다는 결론을 내린 바 있다. 실테조가 오리지널과 동등한 임상적 결과를 만들어 낸다는 의미였다. 인터체인저블 바이오시밀러로 지정되면 의사의 처방없이 약국에서 오리지널 대신 환자에게 제공할 수 있다.
의약품 시장조사업체 이벨루에이트파마는 2026년경 휴미라의 세계 매출이 145억달러(한화 약 18조7950억원) 수준으로 급감할 것으로 분석한 바 있다. 2021년 기준 휴미라의 세계 매출액은 206억 9400만 달러(한화 약 26조8250억원)로 전체 의약품 중 2위를 기록했다.
국내 휴미라 바이오시밀러 개발 업계 관계자는 “자가면역질환 관련 10여 가지 적응증을 가진 휴미라의 매출 감소 여파를 최대한 방어하기 위해 애브비가 세부 적응증 관련 약물의 종류를 늘릴 전략을 세워 실행하고 있는 것”이라며 “여러 자가면역질환 치료제를 확보한 애브비이기 때문에 가능한 전략이다”고 설명했다.
 | | 미국 애브비는 자사의 자가면역질환 치료제 ‘린버크’(성분명 유파다시티닙)의 적응증 확대하기 위해 성인 크론병 환자를 대상으로 임상 3상을 진행하고 있다.(제공 애브비) |
|
‘스카이리치’ 크론병 확대 성공, ‘린버크’도 관련 임상 3상 中 지난 17일 FDA가 중증도에서 중증의 성인 활동성 크론병 환자에게 스카이리치를 활용할 수 있도록 허가했다. 이로써 스카이리치는 기존 중등도에서 중증 성인 판상 건선과 성인 활동성 건선성 관절염까지 총 3가지 적응증을 확보하게 됐다.
앞선 관계자는 “스카이리치가 소아 크론병 환자까지 쓸 수 있도록 적응증을 확보한 것이 아니기 때문에 휴미라의 자리를 온전히 채우는 데는 한계가 있을 것”이라며 “휴미라 바이오시밀러를 해당 적응증을 포함해 출시할 경우 경쟁의 불씨는 여전히 남아 있다”고 설명했다.
한편 애브비는 새로운 크론병 방어벽을 이미 준비하고 있다. 회사 측은 지난 5월 성인 크론병 환자 대상 린버크의 임상 3상 결과를 발표했다. 해당 임상에 참여한 환자 중 린버크 투약군에서 위약군(15%) 보다 약 2.4배 높은 37%의 임상적 관해가 관찰됐다는 것이다. 애브비 측은 올해 말 FDA에 린버크의 크론병 적응증 승인 신청서를 제출할 예정인 것으로 알려졌다.
린버크는 현재 건선성 관절염과 류마티스 관절염, 궤양성 대장염, 아토피 피부염, 강직성 척추염 등 5가지 적응증을 확보하고 있다. 업계에서는 향후 린버크가 크론병 적응증까지 획득하면 휴미라의 적응증을 절반 가량 확보해 미국 내 관련 매출 공백을 일부 채울 수 있을 것으로 분석하고 있다.




![FDA, CAR-T 치료제 접근 장벽 완화[제약·바이오 해외토픽]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200083b.jpg)



![인투셀, 특허이슈에 장외 하한가…퓨쳐켐, 진단제 국내 품목허가 추진[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071000247b.jpg)
![[임상 업데이트] LG화학, 경구용 희귀비만 신약 2상서 체중 감소 효과](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200105b.jpg)

