팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김유림 기자]
바이오니아(064550)가 RNAi 치료제 개발에 착수한 지 8년이 지나도록 임상 소식이 들려오지 않고 있다. 업계에서는 미국식품의약국(FDA) 승인을 받은 RNAi 치료제들이 공통적으로 사용하고 있는 ‘약물전달체’를 확보하지 못했기 때문으로 추정한다. 바이오니아 측은 “자체 개발한 기술 SAMiRNA가 FDA 허가된 약물전달체보다 훨씬 안전하고 효과가 좋다”고 일축했다.
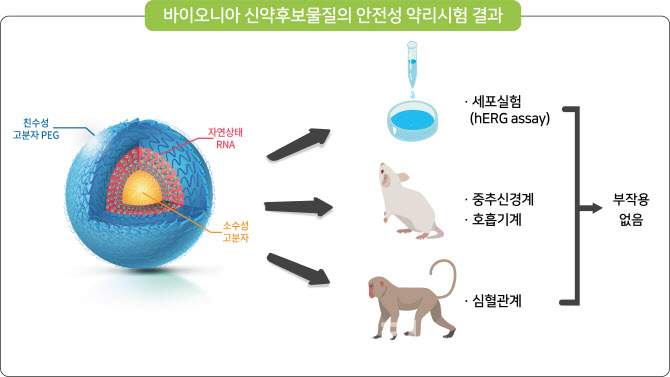 | | 바이오니아 특발성 폐섬유화증 신약후보물질의 안전성 약리시험 결과. (제공=바이오니아) |
|
바이오니아의 RNAi 치료제 개발은 지난 2014년으로 거슬러 올라간다. 당시 바이오니아는 범부처전주기 신약개발사업 과제에서 RNA 간섭(RNA interference, RNAi) 특발성 폐섬유화증(IPF) 치료제 신약 개발 프로젝트를 수행하는 업체로 선정됐다. 2019년 바이오니아는 특발성 폐섬유증 신약후보물질 ‘SAMiRNA-AREG’ 비임상에서 안전성을 입증, 2020년 상반기 중 임상에 들어간다고 발표했다.
하지만 임상 계획은 여러 번 번복됐다. 바이오니아는 당초 시장에 약속한 2020년 상반기를 훌쩍 넘기고 그해 10월 올해 임상 1상을 서울대 의대와 함께 진행한다고 대표 인터뷰를 통해 밝혔다. 이후 2021년 6월 기자간담회에서 올해 임상 1상에 들어간다고 했지만, 지금까지 식품의약품안전처에 임상시험계획서(IND) 제출 소식조차 들려오지 않고 있다.
바이오니아 관계자는 “해외 위탁개발생산(CDMO) 업체를 통해서 임상시험용 의약품의 원료물질을 제조하고 있다. 코로나19 사태 등으로 원료물질 제조 일정이 예상보다 늦어져 아쉽게도 2021년 임상 1상 IND 신청을 못 했다”며 “해외 CDMO 진행 상황을 앞당겨서 빠른 시일 내에 IND 신청을 진행하고자 한다”고 말했다.
반면 업계에서는 바이오니아가 오랫동안 임상에 들어가지 못한 대표적인 원인으로 ‘약물전달체’를 추정했다. 한 바이오회사 대표는 “RNAi 기술에서 중요한 건 인체에 투여한 후 효소에 안 깨져야 되고, 타깃으로 하는 장기로 잘 가야 한다”며 “우선 효소에 깨지지 않게 하기 위해 화학적 변형을 한다. 그다음 문제는 RNAi가 몸 속에서 아무 데나 돌아다니기 때문에 효력이 잘 안 나온다. 이를 해결하기 위해 약물전달체를 붙이게 된 것”이라고 말했다.
이어 “모더나와 화이자 코로나19 백신에 들어가는 지질나노입자(LNP)는 RNAi 치료제 약물전달체로 처음 만들어진 물질이다. RNAi 글로벌 리더들이 개발 초기에는 LNP를 이용했지만, 장기 타깃팅이 잘 안됐다”며 “그러다 새로 발견한 게 간세포에 정확하게 가는 약물전달체 갈낙(GalNAc)이다. 최근 몇 년 사이 글로벌 빅파마가 사들인 RNAi 파이프라인 모두 갈낙을 적용했고, 미국식품의약국(FDA) 허가받은 RNAi 치료제 4개 중 3개가 갈낙이다”고 설명했다.
전 세계에서 상용화에 성공한 RNAi 치료제는 총 4개가 있다. RNAi 글로벌 1위 앨라일람(Anylam)이 2018년 LNP를 이용한 최초의 RNAi 치료제 온파트로(Onpattro)를 내놓았다. 이후 FDA 허가를 받은 기브라리(Givlaari, givosiran), 옥슬루모(Oxlumo, lumasiran), 렉비오(Leqvio, inclisiran)는 약물전달체로 갈낙 기술이 적용됐다.
바이오니아는 글로벌 리더들이 검증한 LNP와 갈낙이 아닌 자체 개발한 기술 SAMiRNA을 사용하고 있다. SAMiRNA(Self Assembled Micelle inhibitory RNA)는 siRNA(짧은 간섭 RNA)를 생체 내 질병 표적장기 세포까지 전달하는 나노입자형 물질이다. 회사 측에 따르면 SAMiRNA 기전은 EPR 효과라는 현상을 이용한다. 특발성 폐섬유화증 환자의 염증부위 혈관 내벽은 헐거워지고 틈새가 넓어지는데, 그 벌어진 틈새로 약물이 빠져나가서 타겟팅을 가능하게 하는 것이다. 섬유증 질환, 고형암 치료에 적합하다고 강조한다.
다만 일각에서는 EPR 효능에 대해서 의문을 제기한다. 익명을 요구한 증권사 바이오 애널리스트는 “EPR 효과는 이미 1980년대 나온 개념이다. 모든 질병 조건을 똑같이 설정하는 동물실험에서는 효과가 나오는데 사람을 대상으로 하는 임상에서는 입증하기가 까다롭다”며 “예를 들어 특발성 폐섬유증은 질환의 정도에 따라 모든 환자의 혈관 상태가 다르다. 어떤 환자의 혈관 틈새는 약물이 많이 빠져나가고, 어떤 환자는 혈관이 덜 헐거워서 조금 빠져나간다. Pk(약물 잔존), pd(약물 효과) 컨트롤이 힘들기 때문에 통계적으로 입증하기 만만찮다”고 말했다.
바이오니아 측은 pk/pd 컨트롤 의문과 관련해 “문제없다”고 일축했다. 회사 관계자는 “혈액 내에서는 4~5시간 내에 다 빠지고, SAMiRNA가 들어간 세포 내에서는 siRNA와 RISC(RNA 유도억압체)가 결합하면 뉴클레아제가 siRNA 분해를 못 시키기 때문에 siRNA+RISC가 지속적으로 유지되면서 타깃 mRNA를 파괴하는 효과가 1개월간 지속된다”고 설명했다. 그러면서 “앨라일람과 아이오니스(Ionis) 신약 파이프라인은 간과 연관된 질환들을 대상으로 개발하고 있다. 반면 SAMiRNA는 간조직 이외에도 암조직과 염증 및 섬유화조직에 보다 선택적으로 흡수되는 특성을 가지고 있다. 가장 치명적인 문제인 선천면역 관련 부작용도 나타나지 않는다”고 덧붙였다.







![유틸렉스, 임상 기대감에 上...에이비온은 3일 연속 상한가[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/06/PS25063000097b.jpg)


![[임상 업데이트] 동아에스티, ADC 신약 ‘DA-3501’ 1상 신청](https://image.edaily.co.kr/images/vision/files/NP/S/2025/06/PS25062800189b.jpg)