[이데일리 김진수 기자] 파로스아이바이오가 이르면 내년에 상장 후 첫 기술수출 계약을 체결할 수 있을 것으로 기대된다.
21일 한국거래소에 따르면 파로스아이바이오는 오는 27일 상장을 앞두고 있다. 상장을 통해 확보한 자금은 연구개발에 투자하고, 파이프라인의 기술이전 및 조기 상용화를 통해 본격적인 매출을 올린다는 전략이다.
 | | 파로스아이바이오 파이프라인. (표=파로스아이바이오) |
|
파로스아이바이오는 현재 PHI-101, PHI-201, PHI-301, PHI-401, PHI-501 등 총 5개의 신약 후보물질을 보유하고 있다. 이 중 상업화 임상 속도가 가장 빠른 PHI-101의 기술수출이 기대되는 상황이다.
급성골수성백혈병(AML)은 혈액세포를 생성하는 줄기세포인 조혈모세포가 악성세포로 변하는 혈액암이다. 악성세포가 골수에서 증식해 간·장·림프선 등 전신에 퍼지는 희귀질환이다. AML 환자는 일반적으로 여러 유전자 변이를 가지고 있는데, 전체 환자 중 약 35%는 FLT3 변이를 보인다.
PHI-101은 ‘FLT3 단백질 저해제’로 현재 국내와 호주에서 AML 환자 대상 임상 1상이 진행 중이다. 1차적으로는 약물 내성 돌연변이를 포함해 FLT3 돌연변이를 가진 불응성·재발성 급성골수성백혈병 환자를 타깃으로 한다.
파로스아이바이오가 실시한 임상 1상 결과에 따르면 28일 주기로 PHI-101을 매일 투여한 FLT3 변이환자에게서 악성골수세포가 평균 87%이상, 최대 98% 줄었다.
FDA 승인 제품 대비 변이에서 효과 현재 FDA 승인을 받은 FLT3 저해제는 아스텔라스의 ‘조스파타’(성분명 길테리티닙)와 다이이찌산쿄의 ‘반플리타’(성분명 퀴자티닙)가 있다. 이 중 반플리타는 이달 20일 품목허가를 획득한 만큼 현재 AML 환자에게 처방되는 FLT3 저해제는 조스파타가 유일하다.
FLT3 저해제의 대표격인 조스파타의 임상 3상 결과를 살펴보면, 투약 환자의 약 30.5%가 재발을 경험한 것으로 나타났다. 또 FLT3-TKD의 돌연변이 중 ‘D835’와 ‘F691’로 인한 약물 내성 문제가 발생했다.
반면, PHI-101은 동물실험에서 경쟁 약물 대비 FLT3로 인한 모든 돌연변이에 높은 효능을 보였다. 특히 약물에 대한 내성을 가진 돌연변이 ‘D835’와 ‘F691’를 가진 암세포에서 조스파타 또는 반플리타 투여군 보다 암세포 성장 억제효과가 최소 2배에서 최대 10배 높은 것으로 확인됐다.
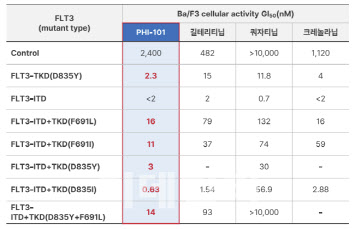 | | 파로스아이바이오 PHI-101과 경쟁약물의 FLT3 변이세포 성장 억제 효과. (표=파로스아이바이오) |
|
파로스아이바이오가 진행 중인 PHI-101 임상 1상의 경우 임상 대상의 반 이상은 기존 FLT3 약물에 불응했던 AML 환자인 만큼, 사람 대상 연구 종료 후 긍정적인 결과를 확인할 수 있을 것으로 기대된다.
독성 검사에서 PHI-101는 소화기관·뇌·조혈기관·비장·가슴샘 등 5개의 장기에서 독성 소견을 보였으나, 조스파타의 경우 소화기관·면역계·조혈기관·눈·신장·간·폐·눈물샘·비뇨기계 등 9개 장기에서 독성 소견이 나타나 안전성 측면에서 경쟁력도 확보했다.
파로스아이바이오 관계자는 “기존 FLT3 저해제를 투여했을 때 치료 효과를 보지 못했던 환자들에게서 효능을 확인 중으로, 기존 약물 약점을 극복하는 차세대 Best-in-class FLT3 저해제가 될 것”이라고 강조했다.
임상 1상 종료 이후 본격 기술수출 기대 파로스아이바이오는 올해 안으로 PHI-101의 AML 임상 1상을 마친다는 계획으로, 기술수출 시기는 임상 1상 데이터를 확보한 이후가 될 것으로 예상된다. 올해 말 임상을 종료할 예정인 만큼 최종 결과 보고서 수령 시점 등을 고려하면 이르면 내년말 또는 2025년 초에 기술수출 가능성이 높은 셈이다.
특히, PHI-101은 2019년 FDA로부터 급성골수성백혈병에 대한 희귀의약품 지정 승인을 받았다는 점에서 기술수출 시점은 더 빠를 것으로 예상된다. 희귀의약품으로 지정된 경우 임상 2상 후 조건부 품목허가 획득이 가능하기 때문에 임상 1상 이후부터 본격적인 협상이 이뤄질 전망이다. 기술수출 계약 협상에서도 유리하게 작용해 더 높은 부가가치를 보장받을 수 있을 것으로 보인다.
파로스아이바이오는 PHI-101의 기술수출을 통해 계약금 약 805억원에 단계별 기술료(마일스톤) 624억원 등 총 1429억원 가량의 매출을 올릴 것으로 기대 중이다.
파로스아이바이오 관계자는 “PHI-101는 임상 2상 완료 후 조건부 품목 허가를 통해 빠른 상용화가 가능한 제품”이라며 “향후 글로벌 제약사에 기술이전을 통해 마일스톤과 로열티 수입을 기대하고 있다”고 말했다.
한편, AML 치료제 시장은 2018년 약 8800억원 규모에서 2028년 3조7000억원까지 성장할 것으로 기대된다. 이 중 FLT3 저해제만 두고 봤을 때 2022년 기준 전세계 시장 규모는 약 4644억원이며, 2032년까지 연평균 7.3%씩 성장해 2032년에는 9384억원의 시장을 형성할 것으로 전망된다.
국내에서는 파로스아이바이오 외 한미약품이 FLT3 저해제 계열 AML 치료제를 개발 중에 있다.







![[르포] 안드로이드 탄생한 보스턴CIC가보니…"K-바이오, 빅딜 마중물"](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071401146b.jpg)
![이승호 데일리파트너스 대표 “하반기 바이오 전망 밝다, 다중항체 주목”[바이오 VC 집중조명]①](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071500005b.jpg)


![[임상 업데이트] LG화학, 경구용 희귀비만 신약 2상서 체중 감소 효과](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200105b.jpg)