팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김지완 기자]
아이큐어(175250)가 파스 치매약을 앞세워 2300억원 규모의 알약 도네페질 시장을 정조준했다.
 | | (갈무리=김지완 기자) |
|
28일 제약·바이오 업계에 따르면, 아이큐어 도네페질 패치제가 오는 8월 시판될 예정이다. 현재 아이큐어는 건강보험심사평가원(심평원)과 도네페질 약가 협상이 진행 중인 것으로 알려졌다.
앞서 아이큐어는 지난해 11월 식품의약품안전처(식약처)로부터 도네페질 패치제에 대해 품목허가를 받았다. 도네페질 패치제는 알약을 파스 형태로 제형을 변경한 것이다.
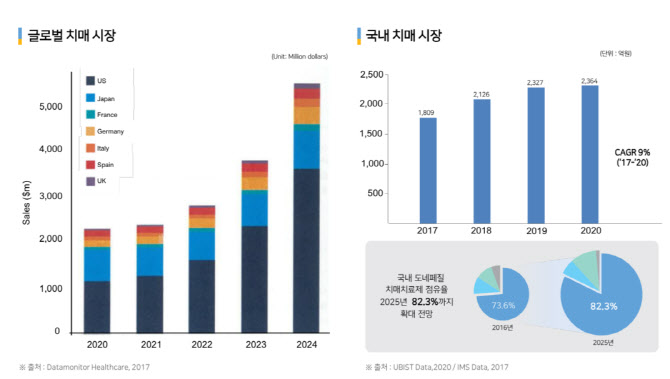
2300억 韓도네페질 시장 정조준 도네페질은 치매 치료제로 인지기능 개선에 도움을 준다. 국내 도네페질 시장 규모만 2300억원에 이른다. 문제는 도네페질 알약 복용에서 오심, 구토, 구역감, 설사 등의 부작용이 빈번하다는 점이다.
아이큐어는 이 같은 문제를 해결하기 위해서 세계 최초로 도네페질 패취제를 개발했다. 아이큐어 관계자는 “먹는 약은 위를 통해 장에서 흡수된다”면서 “구체적으로는 간에서 1차 대사가 일어나고, 모세혈관을 거쳐 전신작용한다”고 설명했다. 이어 “케미컬(알약)이 장기에 부하를 준다”고 덧붙였다. 이어 그는 “반면 패치제는 간을 통과하지 않고 전신작용한다”면서 “장기 부하를 줄이기 때문에 도네페질 경구제의 문제를 상당 부분 줄일 수 있다”고 비교했다.
그럼에도 패치제는 경구약과 유사한 도네페질 혈중농도를 보인다. 더욱이 복용 직후 혈중농도가 급격히 치솟는 알약과 달리, 패치제는 혈중농도가 서서히 상승해 복용 초기 부작용이 최소화된다. 패치제는 일주일에 2번만 붙이면 돼 매일 복용하는 경구제 대비 편의성이 높다.
8월부터 매출 발생...내년 1200억 매출 기대 도네페질 패치제는 당장 8월부터 매출이 발생할 것으로 보인다. 아이큐어가 도네페질 패치제를 생산하면 셀트리온제약이 국내 판매를 전담하는 방식이다. 셀트리온제약은 국내 대형병원 등을 대상으로 영업에 나설 예정이다.
업계에선 초도 유통물량은 20억~30억원 규모에 달할 것으로 추정하고 있다. 연말까지 병원코드 등록이 마무리되면, 내년부턴 본격적인 영업으로 매출 300억~500억원 정도를 올릴 것으로 점쳐진다.
아이큐어 관계자는 “시장 추정치는 상당히 보수적인 수치”라면서 “노바티스 엑셀론의 사례에 근거해 내년부턴 도네페질 패치제 전환율을 50% 이상 예상하고 있다”고 말했다.
노바티스는 지난 2007년 리바스티그민 패치제 ‘엑셀론’을 출시했다. 이 패치제는 출시 첫해 10%, 둘째 연도 50%, 5년 뒤엔 92%로 점유율 높였다. 사실상 같은 성분의 알약 시장을 괴멸시켰다.
이 계산에 도네페질 패치제 예상 매출을 대입하면 올해 230억원, 내년 1200억원, 오는 2026년 2100억원 등이 산출된다. 아이큐어는 지난해 매출 643억원에 283억원의 영업손실을 기록했다. 사실상 패치제가 아이큐어 DNA를 바꿀 잠재력을 가진 셈이다.
FDA IND 받고 美 진출 진행 중 아이큐어 입장에선 국내 도네페질 시장은 쇼케이스에 불과하다는 평가다. 아이큐어는 미국과 유럽이 양분하고 있는 글로벌 도네페질 시장을 겨냥하고 있다. 글로벌 도네페질 시장은 지난 2020년 기준 1조 1000억원 규모로 미국이 35%, 유럽이 30%를 각각 차지하고 있다.
아이큐어는 지난해 4월 도네페질 패치제에 대해 미국 식품의약국(FDA) 임상시험승인(IND)를 받았다. 아이큐어 관계자는 “완주공장 cGMP(FDA 우수의약품 품질관리 기준) 인증 절차를 진행 중”이라면서 “cGM 인증을 받고 나면 올 하반기 임상 약을 미국으로 보내 1상을 개시할 계획”이라고 밝혔다. 이어 “도네페질 패치제 미국 임상은 오는 2024년 상반기에 마무리될 예정”이라며 “같은 해 하반기 FDA 신약허가(NDA) 승인과 cGMP 실사를 거쳐 2025년 미국 출시를 목표로 하고 있다”고 덧붙였다.
아이큐어 측은 도네페질은 이미 허가된 치료제로 임상 1상만으로도 품목허가가 가능할 것으로 내다보고 있다. 아이큐어는 현재 미국 임상과 품목허가를 주도할 파트너 계약을 추진하고 있다. 미국 빅파마와 수차례 미팅을 가지며 기술이전 및 로열티 조건을 협의 중이다.
아이큐어 관계자는 “치매 특성상 알약 복용 여부를 기억하지 못하는 일이 빈번하다”면서 “패치제는 중복 복약 위험을 줄인다. 아울러 치매 환자 중 부작용을 이유로 약을 거부하는 일이 빈번한데, 패치제는 보호자 관라가 용이해 빠른 시장 침투를 기대하고 있다”고 말했다.






![유틸렉스, 임상 기대감에 上...에이비온은 3일 연속 상한가[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/06/PS25063000097b.jpg)


![[임상 업데이트] 동아에스티, ADC 신약 ‘DA-3501’ 1상 신청](https://image.edaily.co.kr/images/vision/files/NP/S/2025/06/PS25062800189b.jpg)