팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김지완 기자]
바이오니아(064550)가 탈모화장품 코스메르나의 국내 출시를 눈앞에 두고있다. 표면상 코스메르나의 기능성 화장품으로 국내 출시가 확정됐지만, 광고마케팅에선 상당한 제약이 따를 것으로 관측된다.
 | | 25일 의약품안전나라에 고시된 코스메르나 탈모 기능성화장품 보고. (제공=식약처 의약품통합정보시스템) |
|
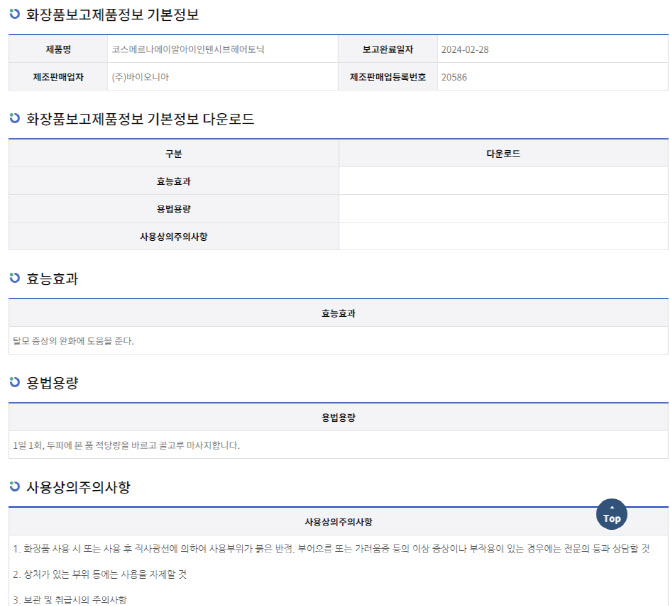
25일 식품의약품안전처(식약처) 의약품통합정보시스템인 ‘의약품안전나라’에 따르면, 지난 2월 28일 바이오니아의 ‘코스메르나 에이알아이 인텐시브 헤어토닉(코스메르나)’의 기능성화장품제품정보 보고가 완료됐다.
코스메르나는 바이오니아의 짧은간섭 RNA(siRNA) 기술이 적용된 탈모 기능성 화장품이다. 탈모 단백질을 만드는 유전 정보를 가진 mRNA(메신저리보핵산)를 분해하는 방식으로 작동한다. 남성형 탈모에 탁월한 효과를 내는 것으로 알려졌다. 기존 탈모약이 모낭세포를 파괴하는 남성호르몬(DHT) 생성을 억제해 여성 사용이 제한되고, 성기능 장애를 일으키는 것과는 구분된다.
바이오니아는 코스메르나에 대해 기능성 화장품 심사 신청을 냈다. 하지만 식약처는 2021년 말 siRNA는 의약품에 준한다고 판단한다며 반려했다. 이후 바이오니아는 식약처를 상대로 제기한 기능성화장품 심사신청 반려처분 등에 대한 행정소송을 제기했다. 하지만 지난 1월 1심에서 패소했다.
바이오니아는 코스메르나 국내 출시가 막힌 사이, 지난해 5월 유럽에서 제품 출시를 먼저 진행했다. 코스메르나는 지난해 8개월 간 17억원의 매출을 기록했다.
소송 패소 1달만에 제품 출시 행정절차 마쳐, 어떻게? 불과 두 달 여전 행정소송에서 패했던 바이오니아는 지난달 코스메르나의 탈모 기능성화장품 출시를 위한 행정절차를 마쳤다. 대단한 반전이 아닐 수 없다.
회사 측에 확인한 결과, 빠르면 5월 중 제품 출시가 이뤄질 것이란 답변이 돌아왔다.
하지만 코스메르나의 제품 성격이 처음 출시를 기획했을 때와는 상당한 차이가 있는 것으로 확인됐다.
중견 화장품업체의 한 품질연구원은 “기능성 화장품은 크게 심사, 보고 두 가지로 나뉜다”면서 “새로운 성분으로 탈모 기능성화장품을 출시하려면 식약처 심사를 받아야 한다”고 설명했다. 이어 “이 경우 안전성과 유효성을 입증하는 방대한 자료를 식약처에 제출해야 한다”고 덧붙였다. 코스메르나는 이 심사 절차를 통과하지 못했다.
해당 품질연구원은 “그렇다고 해서 기능성화장품 출시가 완전히 막히는 것은 아니다”며 “보고라는 절차가 있다. 하지만 이는 식약처가 고시한 원료를 주성분으로 사용해서 제조해야 한다”고 설명했다. 이어 “고시 성분을 쓰면 안전성 자료 제출은 면제 받는다”고 부연했다.
식약처는 ‘탈모 증상 완화에 도움을 주는 기능성 화장품 각조(제2조 제9호 관련)’를 통해 기능성화장품 주성분을 고시하고 있다. 해당 성분은 덱스판테놀, 비오틴, 엘-멘톨, 징크피치리온, 징크피치리온액(50%) 등 총 5가지다.
그는 “해당 성분을 주성분으로 이용해 탈모화장품을 제조하면 식약처 보고 절차만으로 기능성화장품을 출시할 수 있다”고 말했다.
OEM·ODM 개발 탈모화장품에 siRNA 첨가 유력 코스메르나의 경우 다른 경로를 이용했을 가능성도 있다.
연구원은 “기존 화장품 제조업체에서 탈모 기능성화장품으로 심사받아 통과한 제품이 있다면, 주성분은 그대로 둔 채 코스메르나의 부원료(siRNA)를 첨가하는 방식으로 우회할 수 있다”면서 “이 경우도 식약처 보고 절차만으로 제품 출시가 가능하다”고 말했다.
 | | 기능성화장품 심사에 관한 규정. (제공=식품의약품안전처고시 제2023-61호) |
|
그는 “바이오니아의 경우, 화장품제조업이 아닌 화장품책임판매업체”라며 “한국콜마, 코스맥스 화장품 위탁제조가 직접 개발해 심사를 통과한 탈모 기능성화장품을 이용했을 가능성이 높다”고 추정했다.
연구원은 “이 경우 앞서 언급한 5개 주성분이 아닌 다른 성분이 주성분이 될 수 있다”며 “여기에 바이오니아의 siRNA를 부원료가 첨가했을 것”이라고 판단했다. 이어 “구체적으로 바이오니아가 생산한 부원료를 제조업체에 전달하면, 제조업체가 기존 제품에 siRNA 성분을 첨가해 탈모화장품을 위탁생산하는 것이 유력하다”고 덧붙였다.
바이오니아는 코스메르나의 핵심 원료를 생산하는 관련 장비 10대를 보유 중이다. 장비당 연간 생산량은 24~36㎏으로, 매출액 기준 3120~4680억원에 달한다. 이에 업계에선 바이오니아가 화장품제조업으로 판단했지만, 화장품책임판매업으로 지난 2020년 4월 16일 허가받은 것으로 확인됐다. 화장품법 제2조2의 따르면, 화장품제조업, 화장품책임판매업, 맞춤형화장품제조업 등 3종류로 구분한다.
탈모방지 siRNA가 부원료가 돼도 제품 자체는 크게 달리지지 않을 것으로 보인다.
해당 연구원은 “미백, 주름개선 등의 일부 화장품군을 제외하면 주성분 사용 비율이 정해지지 않았다”면서 “주성분 사용비율이 정해져 있다고 하더라도 화장품 특성상 그 비율은 0.4%~2% 이내”라고 설명했다.
그는 이어 “주원료를 얼마만큼 사용하느냐는 그 회사의 기술 노하우 영역”이라며 “가령 경쟁사보다 주성분을 1/10만 쓰고도 동일한 효능을 낼 수 있으면 그만큼 기술력이 뛰어나다는 의미로 평가받는다. 회사는 주성분을 얼마를 쓰던 임상 자료로 효능만 입증하면 된다”고 덧붙였다. 코스메르나의 수출 및 내수 제품 간 품질 차이는 없단 얘기다.
siRNA 효능 광고 제한, 제2의 비에날씬? 글쎄 코스메르나 국내 출시 경로 변경 과정에서 파생되는 문제는 광고·마케팅 영역에서 발생할 것으로 보인다.
연구원은 “현재 국내법상 기능성화장품은 주성분으로만 광고·마케팅이 가능하다”며 “siRNA로 탈모 기능성화장품 심사를 통과한 것이 아니기 때문에 해당 성분으로 광고, 마케팅이 불가능하다”고 지적했다.
앞서 업계에선 코스메르나의 국내 출시가 이뤄질 경우 제2의 비에날씬이 될 수 있다는 관측이 나왔었다. 비에날씬은 바이오니아 자회사 에이스바이움이 제조·판매 중이다. 비에날씬은 지난 2018년 매출이 22억원에 불과했지만, 지난해 매출은 2345억원으로 퀀텀 점프했다. 이 배경엔 홈쇼핑을 중심으로 BNR17 이라는 다이어트 유산균과 관련된 과학적 입증자료(논문, 학술대회, 임상결과) 등을 대대적으로 홍보했기 때문이다. 결론적으로 코스메르나는 비에날씬과 같은 마케팅을 국내에서 할 수 없단 얘기다.
바이오니아 관계자는 “코스메르나 국내 출시와 관련해 오는 28일 주총에서 박한오 회장이 직접 밝힐 예정”이라며 “이전까지 구체적인 사실에 대해 밝히긴 곤란하다”며 말을 아꼈다. 이어 “다만, 홍보실에서도 관련 보도자료를 준비 중”이라고 귀띔했다.




![[생생확대경]삼천당제약 사태가 남긴 질문 셋](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26040700121b.jpg)



![지놈앤컴퍼니, 임상 본격화 기대감에 급등…숨고르기 들어간 바이젠셀[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26043000447b.jpg)

