팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 석지헌 기자] 면역·염증 질환 치료제 개발사 에빅스젠이 글로벌 미충족 의료 수요(global unmet needs)가 높은 점안제형 황반변성 치료제 시장에 도전장을 내밀었다. 현재 주사제형만 있는 16조원 규모 황반변성 시장에서 에빅스젠의 점안제형 치료제가 새로운 트렌드로 자리잡을 수 있을지 관심이 모인다.
유지창 에빅스젠 대표는 지난 11일 이데일리와 만나 “국내 황반변성 치료제 신약으로 환자 대상 안전성과 유효성을 확인한 것은 에빅스젠 AVI-3207이 유일하다”며 “점안제 형태로 투여한 비임상 효력 시험에서 뛰어난 망막투과능과 황반변성 치료효과를 보여 미충족 의료 수요를 해소할 수 있다”고 자신했다.
 | | 유지창 에빅스젠 대표.(제공= 에빅스젠) |
|
에빅스젠은 2000년에 유지창 가톨릭대학교 의과대학 교수가 설립한 면역 및 염증 질환 치료를 위한 신약 개발사다. 지난 2020년 말 기술특례상장을 통한 코스닥 시장 상장 입성에 도전했지만 기술성 평가 관문을 넘지 못했다. 이후 회사는 다양한 파이프라인 개발 과정에서 진전을 보인 만큼 내년 하반기 기술성 평가에 재도전한다는 계획이다.
회사는 질환 특이적인 새로운 타깃과 물질, 기전을 발굴하고 효율적으로 전달하는 기술 플랫폼인 ‘3NASED’를 바탕으로 파이프라인 7개를 개발 중이다. 대표적 파이프라인으로는 점안제형 습성 황반변성 치료제 ‘AVI-3207’이 꼽힌다. 아일리아, 루센티스 등 기존 VEGF 주사 치료제는 고혈압이나 출혈을 동반한 부작용들이 종종 보고되는데, AVI-3207은 이러한 부작용이 없다는 게 그의 설명이다. 에빅스젠은 올해 안으로 식품의약품안전처에 임상1상 시험계획서(IND)를 제출할 예정이다.
유 대표는 “점안제형은 눈에 직접 찌르는 주사제보다 투약 편의성이 높고, 경구용 치료제보다 치료 효과를 즉각적으로 확인할 수 있다는 특징이 있다”며 “현재 글로벌 시장에서 미국 식품의약국(FDA)와 유럽의약품청(EMA) 허가를 받은 점안제형 황반변성 치료제가 없는 상황에서 AVI-3207이 새로운 트렌드가 될 수 있다”고 강조했다.
에빅스젠은 AVI-3207을 주사제형으로도 개발 중이다. 임상1상에서 기존 치료제 대비 적은 주사량과 주사 횟수에도 시력이 개선된 것을 확인했고 기존 항 VEGF 약물 내성 환자 대상으로도 효과를 나타냈다는 설명이다. 올해 12월 임상1상 CSR(최종결과보고서)을 수령할 예정이며 내년 중순 식약처에 임상2a상 시험 IND를 제출할 예정이다. 이와 함께 기술이전도 협의 중이다. 국내 대형 제약사와 공동개발을 협의하고 있으며 다수 글로벌 제약사들과 사업화 논의를 진행 중이라고 밝혔다.
마켓리서치에 따르면 글로벌 황반변성 치료제 시장 규모는 2020년 89억 달러(약 12조7600억원)에서 연평균 8.9% 성장해 2027년에는 153억 달러(21조9400억원)에 이를 전망이다. 2022년 현재 시장 규모는 16조원 규모로 알려져 있다. 에빅스젠에 따르면 해외에서 현재 임상을 진행 중인 점안제형 황반변성 치료제 개발사는 판옵티카(PanOptica)가 있다. 판옵티카의 ‘PAN-90806’은 임상2상 결과 환자 51%에서 유효성을 확인했다. 현재 용해도를 높이는 방향으로 제형을 바꿔 임상2상을 진행하고 있다.
에빅스젠이 보유한 파이프라인 중 가장 속도가 빠른 것은 안구건조증 치료제 ‘AVI-4015’다. 안구건조증 신규 분자 표적인 DDR1 수용체를 억제하는 기전이다. AVI-4015는 현재 국내에서 임상2상을 진행 중이며, 내년 2분기 FDA 2a상 IND 접수를 계획하고 있다.
유 대표는 “임상1상에서 유의한 부작용이 발견되지 않아 작열감, 이물감, 충혈 등 기존 안구건조증 치료제의 부작용을 극복할 수 있을 것으로 기대되는 혁신 신약”이라며 “국내의 노터스사와 공동개발 및 특허사용권 계약을 맺어, 기술료 10억원을 선수취했고, 잠재적인 글로벌 파트너사와 사업화 논의를 진행하고 있다”고 말했다.
회사는 이밖에도 아토피 피부염 치료제 ‘AVI-3307’, 퇴행성 뇌질환 치료제 ‘AVI-6110’, 폐섬유증 치료제 ‘AVI-1001’ 등도 개발 중이다.
유 대표는 “황반변성과 안구건조증 치료제는 내년 중 기술수출하는 것이 목표”라며 “아토피 피부염이나 뇌질환 치료제 등 다른 파이프라인에 대해서도 순차적으로 매년 하나씩 기술수출을 진행한다는 포부를 갖고 있다”고 말했다.
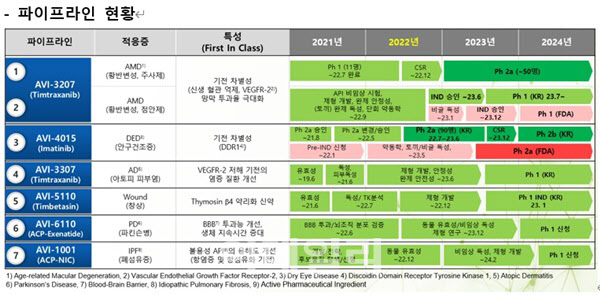 | | 에빅스젠 파이프라인.(제공= 에빅스젠) |
|








![브릿지바이오 26%↑…에스티팜 수주 잭팟[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25070200539b.jpg)


![[AI헬스케어]네이버, 음성인식 기반 생성형 AI 의료 서비스 출시 임박 外](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/06/PS25062900194b.jpg)