팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 송영두 기자] 글로벌 제약사 로슈가 개발한 알츠하이머 조기진단 검사법이 최근 세계 최초로 미국 식품의약국(FDA) 승인을 받았다. 세계 최대 시장에서 알츠하이머 조기진단 검사법이 상용화 물꼬를 트면서 관련 시장이 확대될 전망이다. 특히 국내 조기진단 기업들이 개발한 알츠하이머 조기진단 기술은 로슈 검사법 대비 훨씬 경쟁력이 높아, 시장 확대에 따른 수혜를 누릴 것이라는 분석이다.
3일 제약바이오 업계에 따르면 로슈진단은 알츠하이머 진단 검사 일렉시스(Elecsys) 2종에 대한 미국 FDA 승인을 획득했다. 일렉시스는 뇌척수액(CSF)을 활용한 검사법이다. 이번 승인으로 세계 최초 알츠하이머 뇌척수액 검사법이라는 타이틀을 획득했다. 이에 따라 업계는 알츠하이머신약 승인과 더불어 조기진단 시장 확대를 점치고 있다.
특히 알츠하이머 조기 진단 분야에서는 국내 기업들이 강점을 보이는 만큼 미국 시장 진출시 상당한 시장 잠식이 예상된다는 분석이다. 조기진단 업계 관계자는 “로슈가 승인받은 알츠하이머 진단 검사는 뇌척수액을 활용한 것으로, 이런 검사법은 국내에서도 이미 사용되고 있다”면서 “하지만 환자들이 검사를 기피하는 경향이 높다. 침습적인 방식이 환자에게 부담으로 이어지면서 일반적인 검사법으로 이어지기에는 쉽지 않다. 뇌척수액이 아닌 다른 방식의 진단검사법에 기회가 열릴 것”이라고 말했다.
세계 최초 뇌 MRI 진단 제품, 올해 FDA 승인 유력 현재 알츠하이머를 확진할 수 있는 검사는 없다. 다만 주로 인지기능검사에 크게 의존하고 있다. 잉크우드 리서치에 따르면 알츠하이머병 시장 규모는 2025년 약 8조5298억원(연평균 5.69% 성장)에 달한다. 이중 알츠하이머 진단 시장은 연평균 4.45% 성장해 2025년 약 1조9890억원 규모를 형성할 것으로 전망된다. 진단 시장에서 주목받는 분야는 AI를 활용한 분야와 혈액검사 분야다.
최근 인공지능(AI) 의료 분야에서
루닛(328130)과 함께 가장 주목받는 기업인
뷰노(338220)는 AI를 활용한 MRI 진단 시장을 정조준하고 있다. 이 회사는 뷰노 딥브레인 AD 솔루션을 개발해 뇌 MRI 기반 알츠하이머 진단 제품을 내놨다. 해당 제품은 3차원 뇌 MRI 영상을 분석해 뇌 영역별 부피, 대뇌피질 두께 변화, 대뇌백질 고강도 신호 등 정량적 정보를 1분내 제공한다. 로슈 진단 검사법은 침을 활용하지만, 이 회사 제품은 영상기기를 활용하고 AI로 정밀분석이 가능하다는 게 장점이 다.
뷰노 관계자는 “뷰노메드 딥브레인은 뇌 MRI를 기반으로 뇌 영역을 100여개 이상으로 분할하고, 주요 뇌 영역의 위축 정도 정보를 제공한다. 의료진이 환자 뇌 영역별 위축 정도의 정상군 대비 비교 수치와 이를 기반으로 계산한 뇌 나이 등을 진단할 수 있다”며 “경도인지장애, 알츠하이머성 치매, 혈관성 치매 등 주요 퇴행성 뇌질환 진단에 활용할 수 있다”고 말했다.
뷰노메드 딥브레인은 올해 FDA 승인을 목표로 하고 있다. 특별한 문제 없이 올해 연말 승인이 이뤄지면 내년 상반기까지 미국 병의원에 신속한 진출을 계획하고 있다. 회사 관계자는 “뷰노메드 딥브레인은 현재 미국 FDA 승인을 위한 절차가 진행 중이다. 빠르면 올해 말 승인될 것으로 기대한다”며 “승인되면 미국 동부쪽 병의원들(뷰노 미국 현지 법인 기반)에 빠르게 진출을 도모할 예정이다. 현지 시장 점유율이나 매출 목표는 구체화 되면 발표할 예정”이라고 강조했다.
 | | (자료=피플바이오) |
|
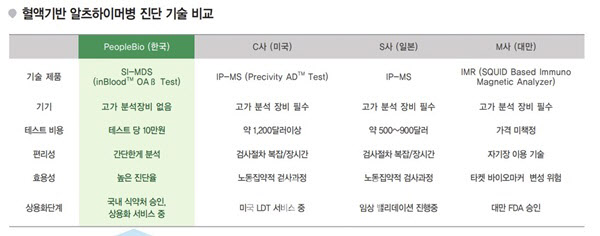
혈액검사시장서 톱티어, 싱가폴-佛 이어 美 진출 추진 피플바이오(304840)는 세계 최초 혈액기반 알츠하이머 조기진단검사를 상용화했다. 이는 MDS(Multimer Detection System) 플랫폼 기술을 기반으로 알츠하이머병 조기 진단에 특화된 기술을 확보했기에 기능했다. MDS 플랫폼은 항원을 겹치게 설계해 변형단백질 질환에서 특징적으로 나타나는 올리고머 및 멀티머를 선택적 구별해 검출하는 기술이다. 모든 변형단백질질환 진단에 적용 가능해, 알츠하이머, 파킨슨병 진단이 가능하다.
특히 알츠하이머 진단제품 ‘inBlood OAß Test’는 로슈 뇌척수액 검사법과 기존 검사법 대비 높은 경쟁력을 갖고 있다. 뇌척수액 검사는 침습 채취로 인한 통증과 실험실간 오차로 명확한 임계치 제시가 불가능하다. 또한 가장 흔하게 사용되는 아밀로이드 PET 검사는 방사선 노출 위험과 고비용에 따른 낮은 접근성이 단점으로 지적된다. 반면 피플바이오 검사법은 △소량 혈액 채취의 비침습적 검사 △간단한 방식으로 환자 및 사용자 편의성↑ △고가 분석장비 필요없어 저비용 공급 가능 등의 경쟁력이 있다.
피플바이오 관계자는 “로슈의 뇌척수액 검사법은 미국에서 자리를 잡지는 못할 것으로 본다. 침습적인 방식으로 가격도 높다”며 “자사 검사법은 알츠하이머 검사 중 가장 니즈가 높은 혈액을 활용한 방식으로 로슈 검사법보다 저렴하면서 편의성도 높아 경쟁력이 있다”고 말했다. 실제로 알츠하이머 진단 시장 중 가장 늦게 열린 혈액검사 시장은 2020년 302억원에서 2025년 1683억원 규모로 연평균 28.5% 성장할 것으로 전망된다. 이는 알츠하이머 진단 분야 중 최고 성장률이다.
피플바이오 측은 미국 시장 진출시 상당한 시장 영향력이 있을 것으로 내다보고 있다. 혈액기반 알츠하이머 조기진단 제품을 개발 중인 곳은 국내 1개사, 일본, 대만 기업이 각각 1개사 등 총 4개사가 있지만, 현재 제품을 상용화한 곳은 피플바이오가 유일하다. 이 회사는 이미 싱가포르, 프랑스 시장에 진출했다. 회사 관계자는 “현재 미국 시장 진출을 위한 컨설팅을 진행 중이다. FDA 허가를 받기 위해서는 임상이 필요한데, 기존 허가 받은 혈액검사 제품이 없어 그런 부분을 컨설팅받고 있다”며 “임상 과정을 거치면 2~3년 내 미국 진출이 유력하다”고 설명했다.







![인투셀, 특허이슈에 장외 하한가…퓨쳐켐, 진단제 국내 품목허가 추진[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071000247b.jpg)
![[임상 업데이트] LG화학, 경구용 희귀비만 신약 2상서 체중 감소 효과](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200105b.jpg)

