[이데일리 김유림 기자]
올리패스(244460)가 비마약성 진통제 신약 OLP-1002 호주 임상 1b상 유의성 확보 실패 공시와 함께 연내 유럽 임상을 진행할 것이라는 입장을 밝혔다. 하지만 P값이 안 나온 호주 임상 1b상을 바탕으로 유럽 임상 2상을 신청하는 것에 대해 의구심이 제기된다. 회사 측은 1상의 안전성 데이터 확보로 2상 신청을 할 수 있다고 해명했다.
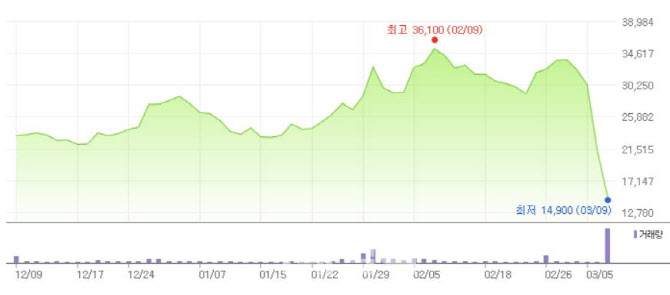 | | 최근 3개월 올리패스 주가 추이. [자료=네이버금융] |
|
9일 금융감독원 전자공시시스템에 따르면 올리패스는 지난 8일 OLP-1002 호주 임상 1b상에서 통계적 유의성을 확보하지 못했다고 공시했다.
위약군의 효능이 약물군보다 2배 이상 높게 나오면서 투자자들에게 P값도 제공하지 못했다. 임상 시험에서 P값은 0.05 이하면 성공, 0.05를 초과하면 통계적 유의성 확보에 실패했다는 것을 의미한다.
하지만 회사 측은 유럽 임상을 진행한다는 보도자료를 배포했다. 올리패스가 공시 직후 배포한 자료에는 “이번 임상을 통해 안전성이 확인된 만큼 신경손상성 통증 환자를 대상으로 한 유럽 임상 2a상 시험과 만성관절염 통증 환자를 대상으로 한 임상 2a상은 예정대로 연내 진행할 것이라고 밝혔다”는 내용을 담고 있다.
금융위원회와 한국거래소 바이오 공시 가이드라인에 따르면 임상 시험과 관련해 회사 관계자의 자의적인 해석은 허용되지 않는다. 식품의약품안전처, 미국식품의약국(FDA), 유럽의약국(EMA) 등 시판허가를 내주는 보건당국에서 인증을 받은 경우에만 가능하다.
올리패스의 연내 유럽 임상 진행은 해당 국가의 승인을 받은 내용이 아니다. 회사 관계자는 “호주 1b상에서 안전성에 이상이 있다는 보고가 없었다”며 “호주 1b상의 안정성과 내약성을 바탕으로 유럽 임상 2a상, 호주 임상 2a상 신청을 준비를 하고 있는 단계다”고 말했다.
이어 “임상 2상을 신청했으면 공시 사항이라서 공시를 했을 것”이라며 “임상 1상 공시하고나서 시장에서 임상 2상 진행에 대한 우려가 나왔고, 이를 해소하기 위해 보도자료를 냈다. 포괄적으로 하반기 내에 진행한다고 얘기한 것”이라고 덧붙였다.
최근 금융 당국은 바이오 기업이 대표 인터뷰, 기자회견, 보도자료 등 공식적인 회사의 발표에서 부풀려진 정보를 제공했다면 허위 공시로 보고 있으며, 투자자들에게 혼선을 줄 수 있는 정보를 제공하면 안된다.
올리패스 측은 “세부적으로는 임상 1상이 최종적으로 마무리한 후 프로토콜을 수립, 임상시험수탁기관(CRO) 계약 등 여러 과정을 거쳐서 임상 2상을 신청할 계획을 갖고 있다고 보면 된다”며 “호주 1상 데이터가 추후 임상 2상을 하기에는 장애물이 되지 않는다. 하반기 내에 진행하는 데 차질이 없다는 뜻이다”고 설명했다.
반면 P값 확보를 못한 호주 1b상 데이터를 통해 유럽 임상 신청을 추진하는 계획에 대한 의구심이 제기된다. 올리패스는 호주 임상 1b상, 아직 결과 발표가 되지 않은 영국 임상 1상의 안전성 데이터를 확보하면 유럽 2a상 승인을 받아 약효를 확인한다는 방침이다.
임상시험 과정에서 ‘임상 1상’은 최대 사용 가능 용량 및 부작용 등 안전성에 대해 파악한다. ‘임상 2상’은 임상 1상에서 정해진 용량을 토대로 환자에게 투여해 본격적으로 약의 효과를 평가하는 단계다. 회사 측은 통상적으로 호주 및 영국 임상 1상 안전성 데이터로 다음 단계의 유럽 임상 계획 승인을 받을 수 있다고 전했다.
호주는 정부 투자의 지원을 받아 첨단 연구개발을 견인하는 세계적인 대학, 연구소와 학군이 자리 잡고 있다. 특히 글로벌 수준의 인프라를 갖춘 주요 병원 및 미국 식품의약국(FDA) 준수 연구를 통해 장기간 축적된 기록을 갖춘 전문 임상시험 센터를 보유하고 있으며, 호주에서 진행한 임상시험은 대외적으로 신뢰도가 높아 미국, 유럽 등 선진국에서도 받아들여진다.
2006년 설립된 올리패스는 독자적으로 개발한 ‘올리패스 인공유전자 플랫폼(OliPass PNA)’을 기반으로 RNA치료제 개발을 전문으로 하는 바이오 기업이다. 올리패스가 개발 중인 비마약성 진통제 OLP-1002는 RNA 조절을 통해 특정 단백질의 발현을 저지해 통증은 없애고, 나머지 감각은 정상으로 유지하는 기전이다.
올리패스의 지난해 매출액은 전년대비 67.8% 증가한 28억6071만원을 기록했다. 다만 영업이익은 전년대비 10.2% 감소한 236억9812만원 손실을 냈다. 회사 측은 “종속기업의 화장품 판매 매출이 증가했으나, 임상비용을 포함하는 연구개발비가 증가하면서 영업손실리 커졌다”고 전했다.






![[르포] 안드로이드 탄생한 보스턴CIC가보니…"K-바이오, 빅딜 마중물"](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071401146b.jpg)
![유한양행 ‘렉라자’ 글로벌 매출 급증에 20% ↑…제넥신·국전약품 上[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071800211b.jpg)
![美FDA, 신약 허가 거절시 보완요구서한 공개[제약·바이오 해외토픽]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071900105b.jpg)

