[이데일리 김지완 기자] GC녹십자와
JW중외제약(001060)이 국내 혈우병 치료제 패권을 두고 연일 난타전을 벌이고 있다.
 | | 헴리브라. (제공=JW중외제약) |
|
두 회사의 자존심 싸움은 GC녹십자가 지난 21일 ‘헴리브라(성분명:에미시주맙) 혈전 이상사례 보고율 8인자 제제보다 2.8배 높았다’는 제목의 보도자료를 배포하면서 논란이 시작됐다.
GC녹십자 측은 헴리브라 이상사례 2383건 중 혈전 이상사례는 97건으로 4.07%에 달한다고 발표했다. 반면, 8인자 제제 이상사례 9324건 중 혈전 이상 사례는 134건으로 1.44%에 불과했다며 논란에 불을 지폈다.
GC녹십자는 이 같은 연구결과를 지난 17~19일 미국 메릴랜드에서 열린 미국출혈장애학회에서 발표했다. 이 연구는 GC녹십자 최봉규 데이터사이언스 팀장과 성균관대학교 약학대학 신주영 교수, 한국혈우재단 부설의원 유기영 원장 등이 공동저자로 참여했다. 이들은 미국 식품의약국(FDA) 이상사례보고시스템(FAERS)에 지난 5년간(2018년~2022년) 헴리브라와 8인자 제제 투여 후 각각 접수된 이상사례 데이터를 기반으로 연구를 진행했다.
JW중외 “세상에 이런 통계가 어딨나” JW중외제약은 곧장 반박에 나서며 GC녹십자 측의 주장을 반박했다.
JW중외제약은 “신약이 출시되면 초기에 이상사례 보고건수가 집중되는 경향이 있다”면서 “환자들도 약이 온전히 검증됐다고 보지 않기 때문에 ‘이거 문제 있는 거 아니냐’라는 생각에 더 적극적으로 이상사례 신고를 하는 경향이 있다”고 지적했다. 이어 “GC녹십자가 내놓은 연구는 이런 앞뒤 상황을 따지지 않고, 특정 시기만 분석한 것”이라고 덧붙였다.
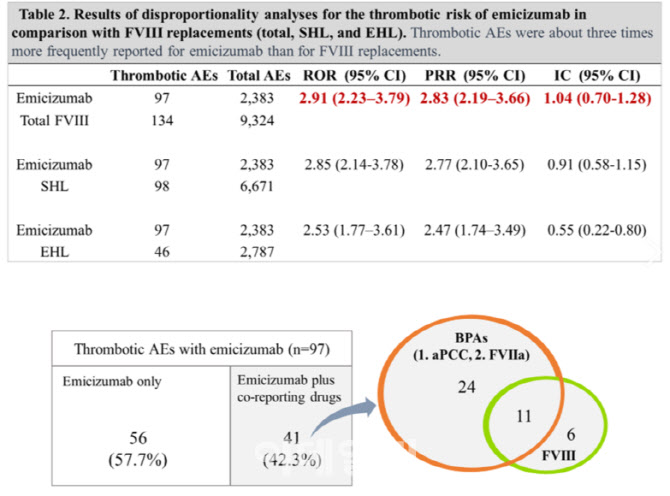 | | GC녹십자가 미국출혈장애학회에서 발표한 포스터 중 일부. (제공=GC녹십자) |
|
특히, JW중외제약은 이번 보고가 총 투여환자 숫자를 알 수 없고, 중복 보고가 여과없이 반영됐다고 꼬집었다. 전체 이상반응 숫자도 8인자 제제는 9324건인데 반해, 헴리브라는 2383건으로 3배 이상 차지가 나는데, 비율만 따지는 건 납득할 수 없는 통계 왜곡이라는 입장이다.
GC녹십자는 JW중외제약에 즉각 재반박하며 수위를 높였다. GC녹십자 측은 “이번 연구가 환자들의 자발적 보고에 기반을 뒀다는 점에서 한계가 있다는 것은 인정한다”면서도 “하지만 보고를 강제하지 않았다는 측면에서 통계 왜곡은 없다”고 잘라 말했다. 그는 이어 “특히, 이번 통계에 포함된 8인자 제제 숫자만 무려 20가지”라며 “20종의 8인자 제제를 통계에 모두 포함하고 있다는 점에서 통계 왜곡이 될 가능성은 극히 낮다”고 강조했다.
CG녹십자 “헴리브라 혈전 문제 제기, 처음 아냐” 양사 간 난타전은 꼬리에 꼬리를 물며 이어지고 있다.
JW중외제약 측은 “헴리브라는 중증 치료제”라며 “반면 8인자 제제는 경중, 중등증 환자도 투약이 가능하다”고 비교했다. 이어 “결론적으로 헴리브라 투약 환자군이 훨씬 더 안 좋은 상태”라며 “그런데도 헴리브라 혈전 발생 비율이 8인자 제제보다 높다고 단순 비교하는 것 자체가 말이 안된다. 환자군 자체가 다른데 어떻게 비교가 가능하냐”며 비판했다.
이에 GC녹십자 측은 “이번 연구가 최초의 연구가 아니란 점을 분명히 한다”며 “지난 3월 유럽에서도 동일한 연구 결과가 나와, 우리가 미국 측, 즉 FDA 자료로 한번 더 검증을 실시한 것”이라고 물러서지 않았다. 이어 “유럽 연구는 우리와 무관한 연구”라고 했다.
해당 논문은 국제저널(Journal of Thrombosis and Haemostasis)에 게재된 ‘에미시주맙 및 확장 반감기 8인자 대체 약물과 관련된 출혈성 및 혈전성 부작용’(Hemorrhagic and thrombotic adverse events associated with emicizumab and extended half-life factor VIII replacement drugs: EudraVigilance data of 2021)을 주제로 발표됐다. 이 논문은 헴리브라가 8인자 제제보다 출혈 보고율은 낮지만, 혈전 보고율이 높다며 우회제인 헴리브라 투여 시 주의(모니터링)가 필요하다고 결론 냈다.
“헤리브라 흠집 내기” 이번 연구 발표가 논란의 중심에 선 이유는 JW중외제약은 헴리브라를, GC녹십자는 8인자 제제인 ‘그린모노’와 ‘그린진에프’를 각각 판매 중이기 때문이다. 결국, 공익적 가치에 따른 순수 과학연구물을 발표한 게 아닐 가능성이 높다는 것이다.
혈우병은 A형은 8번 응고인자가, B형은 9번 응고인자가 각각 없거나 부족해서 발생한다. GC녹십자의 그린모노와 그린진에프는 A형 혈우병 환자의 결핍된 8인자 제제를 보충해주는 방식으로 치료한다. 반면, 헴리브라는 9인자와 10인자를 결합해 8인자를 모방하는 방식이다.
업계 관계자는 “헴리브라가 긴 반감기에 투약 주기가 길고, 8인자를 우회하는 특성으로 내성이 없다는 장점에 시장 점유율이 가파르게 올라가는 추세였다”고 진단했다.
국내 A형 혈우병 환자는 2019년 기준 1749명으로, 시장 규모는 1500억원 내외로 추산된다. 헴리브라는 지난해 매출액이 62억원에 불과했다. 시장 대부분을 8인자 제제가 차지했단 얘기다. 하지만 헴리브라가 지난 5월 급여가 확대되면서 사정이 달라졌다. 헴리브라는 지난 2분기 매출액 44억원을 기록했고, 현재는 월 매출 20억원 수준으로 매출이 확대됐다.
업계에선 헴리브라가 올해 160억원, 내년 300억원의 매출액을 각각 기록할 것으로 내다봤다. 헴리브라가 장기적으론 점유율 70% 이상으로 1000억원의 매출액 달성이 유력하단 전망도 나왔다. 8인자 제제 판매사 입장에선 시장 지키기가 불가피해졌다는 분석이다.
해당 업계 관계자는 “하지만 이번 논란으로 헴리브라가 8인자 제제보다 위험할 수 있단 인식이 생겼다”면서 “GC녹십자의 목표가 헴리브라를 견제하는 것이었다면 성공한 것”이라고 평가했다.
한편, GC녹십자 측은 “이번 연구가 헴리브라를 폄하하기 위한 목적은 아니다”며 “헴리브라는 접종 편의성도 높고 제제의 우수성을 인정한다. 다만, 새로운 치료제이기 때문에 조금 더 검증이 필요한 상황”이라고 했다.







![인투셀, 특허이슈에 장외 하한가…퓨쳐켐, 진단제 국내 품목허가 추진[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071000247b.jpg)


