팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 김지완 기자] 기술수출에 성공한 신약 파이프라인 가운데 기술이전 시점과 비교해 임상단계가 진전한 신약 후보물질은 극소수인 것으로 확인됐다.
31일 클리니컬 트라이얼즈에 따르면, 2020년부터 지난해까지 기술수출 된 치료제 후보물질 79종 가운데 임상단계 진전을 기록한 파이프라인은 11개로 집계됐다. 특히, 기술수출 시점 대비 임상단계가 2단계 이상 진행된 파이프라인은 4개에 그쳤다.
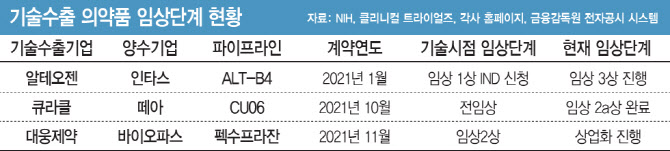
임상단계가 2단계 이상 진행된 파이프라인은 알테오젠 ALT-B4, 큐라클 CU06, 대웅제약 펙수프라잔 등이다. 임상단계가 기술수출 시점 대비 1단계 진전된 곳은 레고켐바이오, 팬젠, 동아에스티, 에이프릴바이오, 한미약품, 제넥신 등이다. 대부분 파이프라인은 임상단계가 기술수출 시점과 비교해 차이가 없었다.
FDA 임상 2단계 진전은 큐라클이 유일 빅파마 기술수출에 미국 식품의약국(FDA) 임상이 2단계나 진전한 곳은 큐라클과 올릭스 뿐이다. 이들은 공교롭게도 계약 상대방이 모두 프랑스 안질환 전문제약사인 떼아와 맺었다.
떼아는 세계 80여 개국에 1500여 종의 안과 의약품을 판매 중이다. 안질환 치료 시장에서 유럽 3위, 세계 9위를 각각 차지하고 있다. 떼아의 2021년 연매출액은 6억 9000만유로로 집계됐다. 떼아는 세계 30여 개국에 자회사를 두고 있다.
큐라클(365270)은 지난 2021년 10월 프랑스 떼아에 당뇨병성 황반부종 및 습성 황반변성을 적응증으로 하는 CU06을 기술이전했다. 이 치료제는 기술수출 당시 동물실험(전임상) 단계였으나 최근 미국 식품의약국 (FDA) 임상 2a상을 완료했다. CU06 임상 2a상 결과는 올 1분기 중으로 나올 예정이다. 큐라클은 올 7~8월경 CU06 FDA 임상 2b상을 진행할 계획이다.
알테오젠·대웅제약, 신흥국 임상 2단계 진전 알테오젠(196170)과
대웅제약(069620)은 신흥국 임상에서 기술수출 시점보다 임상진전을 이룬 경우다.
알테오젠은 2021년 1월 7일 인도 소재 인타스 파마슈티컬스와 ALT-B4에 기술수출 계약을 체결했다. 인타스 파마슈티컬스는 인도에 본사를 둔 제약 회사로, 전 세계 85개국 이상에서 복제약 사업을 하고 있다. 연간 매출은 2조원 정도이며, 매출의 69% 이상이 EU, 미국 등 해외에서 발생한다.
ALT-B4의 기술수출 시점의 임상단계는 1상 임상시험단계(IND)였고, 현재 임상 3상을 진행 중이다. ALT-B4는 알테오젠이 개발한 인간 히알루로니다제 효소 단백질로, 정맥주사로 투여해야 하는 바이오의약품을 피하주사로 바꿀 수 있는 기술이다. 이 기술은 주사 시간을 단축하고 통증과 부작용을 줄이는 등 환자 투약 편의성을 높이는 장점이 있다.
알테오젠은 인타스에 ALT-B4를 이용해 바이오 제품 2개를 피하주사제로 개발하고 상용화할 수 있는 권한을 부여했다. 알테오젠은 인타스로부터 계약금 600만달러(약 66억원)와 향후 제품의 임상 개발, 판매 허가, 판매 실적 등에 따른 단계별 기술료 (마일스톤)로 최대 1억900만달러(약 1200억원)를 받을 수 있다. 또 상용화 시 매출에 따른 로열티를 받게 된다.
펙수프라잔은 대웅제약이 자체 개발한 위식도 역류질환 치료 신약이다. 이 약물은 위벽에서 위산을 분비하는 양성자 펌프를 차단하는 ‘칼륨 경쟁적 위산 분비 억제제’ (P-CAB) 계열로, 기존의 위산 분비 억제제보다 빠르고 강력하게 작용한다.
대웅제약의 위식도역류질환 치료제 펙수프라잔 역시 임상단계가 빠르게 진행 중인 것으로 확인됐다. 대웅제약이 2021년 11월에 바이오파스와 콜롬비아, 에콰도르, 페루, 칠레 등 중남미 4개국 판권에 대해 340억원 규모의 계약을 각각 체결했다. 계약 당시 펙수프라잔은 임상 2상이었는데, 현재는 상업화 단계다.
대부분 임상진전 젠걸음…이유는 제각각 FDA·신흥국 임상여부를 떠나 임상진전이 되는 경우는 그나마 나은 상태다. 대부분 기술수출 신약 후보물질의 임상은 정체 상태다.
한 임상 전문가는 “(치료제) 임상시험 과정에서 예상치 못한 안전성 문제나 예상보다 낮은 효능이 드러날 수 있다”면서 “이 경우 임상시험 중단이나 재설계를 필요로 할 수 있다”고 말했다.
해당 임상전문가는 모벤처의 항암제 FDA 임상 진입 예고 시점 대비 2년 이상 지연된 이유가 예상치 못한 독성 문제가 발생했기 때문이라는 사례를 곁들였다.
그는 “기술수출 후 신약 후보물질은 전적으로 기술도입 주도로 이뤄진다”면서 “이 과정에서 의사소통 문제나 전략적 불일치가 발생할 수 있다. 이런 상황에서 임상지연은 불가피하다”고 설명했다.
이 외에도 신약 후보물질이 기술수출 후 임상진전이 더딘 이유로 △계약 상대방(대부분 바이오텍)이 임상 자금 확보에 난항을 겪는 경우 △규제기관 지적에 따라 보완자료 제출이 늦어지는 경우 △임상시험 중 환자모집이 쉽지 않고, 시험진행 자체가 쉽지 않은 경우 △신약개발 과정 중 예상치 못한 기술적 문제 발생으로 추가 연구가 필요한 경우 등이 조사됐다.






![인투셀, 특허이슈에 장외 하한가…퓨쳐켐, 진단제 국내 품목허가 추진[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071000247b.jpg)
![[임상 업데이트] LG화학, 경구용 희귀비만 신약 2상서 체중 감소 효과](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200105b.jpg)

