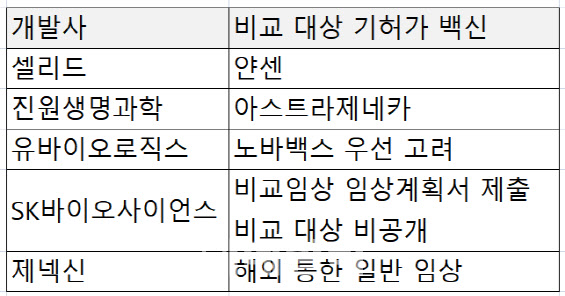
 | | (자료=업계) |
|
[이데일리 노희준 기자] ‘비교임상’을 거칠 것으로 예상되는 국내 코로나19 백신의 수출 전선에 우려가 나오는 상황에서 가장 먼저 임상 3상 시험계획서를 제출한
SK바이오사이언스(302440)도 일단 비교임상 계획을 제출한 것으로 나타났다. 비교임상을 준비중인 국내 회사들은 비교임상이 국내만의 제도가 아닌 데다 임상 실패 위험도 줄일 수 있다고 강조했다. 비교임상은 백신 투약군과 가짜약 투약군의 예방효과를 견주는 일반적인 임상이 아니라 이미 허가된 백신과 개발 중인 백신의 중화항체가와 같은 면역원성 지표를 비교하는 임상을 말한다. 식품의약품안전처는 백신 접종 시작으로 대규모 피험자 모집이 어려운 상황을 감안해 비교임상 방식의 3상도 허용했다.
30일 SK바이오사이언스 관계자는 “코로나19 백신 후보물질 ‘GBP510’의 임상 3상 시험계획서(IND)를 식약처에 비교임상으로 제출했다”며 “다만, 어떤 물질을 대상으로 어떤 임상을 진행할지는 3상 시장 전에 최종적으로 결정할 것”이라고 말했다. 이 회사는 2개 후보물질로 코로나19 백신을 개발 중이다. GBP510 이외에 ‘NBP2001’도 임상을 진행 중이다. 회사는 임상 결과를 고려해 3상에 진입할 최종 물질을 선택하고 임상 방식도 확정할 방침이다. GBP510은 회사가 빌&멀린다게이츠 재단, 전염병대비혁신연합(CEPI) 등의 지원을 받아 미국 워싱턴대학 항원디자인연구소와 공동개발한 물질이다. 회사측은 이번 임상계획을 제출할 때 빌&멀린다게이츠 재단, CEPI와 협의했다고 했다.
SK바이오사언스가 일반 임상 카드를 버리지 못하는 것은 비교임상 데이터를 해외에서 인정받지 못할 수 있다는 우려 때문이다. 면역대리지표(ICP)확립 등 명확한 국제적 가이드라인이 아직 없다는 이유에서다. ICP확립이란 백신의 예방효과와 상관관계가 있다고 판단되는 중화항체가 등의 지표가 일정 값 이상이면 바로 백신 효능을 인정해주는 방법이다. 코로나19는 백신 접종이 시작된 지 6개월밖에 지나지 않아 아직 ICP확립이 안 된 상황이다.
코로나19 백신을 개발 중인 국내 다른 회사들은 비교임상에 대해 좀 더 확고한 입장이다. 얀센 백신과 비교임상을 할 계획인
셀리드(299660) 강창률 대표는 “세계보건기구(WHO)에서도 ICP 확립이 금세 이뤄지지 않는다는 데 어느정도 공감대가 있고 그 대안으로 ‘이뮤노 브릿징 스터디’(immuno bridgding study)라는 용어로 비교임상을 고려 중”이라며 “WHO는 지금 상황에서 (일반 임상으로는) 전세계 특히 저소득국가에 백신을 (개발) 공급하는 게 힘들다고 보고 있다”고 말했다. 다만, WHO에서 비교임상에 대한 공식입장이 나온 것은 아니다.
아스트라제네카 백신과 비교임상으로 임상 3상을 진행할 계획인
진원생명과학(011000)은 비교임상이 실패 위험성을 줄이는 장점도 있다고 봤다. 진원생명과학 관계자는 “국내 승인이 해외 진출에 도움이 될 것”이라며 “(비교임상 후에)일반 임상 3상을 추가로 해야 하더라도 후발주자라는 입장에서 조금 더 늦어지는 것밖에 안 돼 수익성에선 문제가 안 되지만, 처음부터 대규모 임상 3상에 나섰다 실패한다면 그 손실은 막대하다”고 강조했다. 비교임상 3상에는 500억~900억원이 소요되는 것으로 예상된다. 반면 모더나의 경우 3만명을 대상으로 한 임상3상에 8000억원을 쓴 것으로 알려져있다. 유바이오로직스 관계자는 “(적어도)개발도상국이나 중진국에서는 비교임상 데이터를 인정해줄 것”이라며 “개발 중인 합성합원 방식 백신은 메신저리보핵산(mRNA)백신에 비해 싼 데다 콜트체인도도 필요 없고 안전성이 높아 임상에 성공한다면 수요가 클 것”이라고 말했다.
전문가들 의견은 엇갈린다. 김우주 고려대병원 감염내과 교수는 코로나19의 ICP확립이 되지 않아 비교임상만 거친 백신은 수출이 어려울 수 있다고 봤다. 반면 엄중식 가천대 길병원 감염내과 교수는 “비교임상은 우리만의 문제가 아니며 유럽에서도 비교임상으로 갈 수밖에 없는 상황이 생기고 있다”며 “외국에서도 앞으로의 백신 개발 임상연구는 비교임상으로 진행될 수밖에 없다고 생각하고 있어 비교임상이 (수출에) 결정적인 걸림돌이 되지는 않을 것”이라고 말했다. 실제 프랑스 제약사 발네바사는 현재 영국 규제당국의 허가를 받아 아스트라제네카 코로나19 백신과 자사 백신의 비교임상 3상을 진행중이다.







![브릿지바이오 26%↑…에스티팜 수주 잭팟[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25070200539b.jpg)


![[AI헬스케어]네이버, 음성인식 기반 생성형 AI 의료 서비스 출시 임박 外](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/06/PS25062900194b.jpg)