[이데일리 노희준 기자] “제대혈(탯줄 속 혈액)에 있는 줄기세포를 20년 동안 연구해왔습니다. 줄기세포에서 얻은 개발 기술과 경험을 앞으로는 면역세포에 적용해 더 좋은 면역항암제나 자가면역질환 치료제를 개발하려고 합니다.”
최근 제대혈 유래 면역세포치료제를 개발하는 자회사(이뮤니크)를 설립한 양윤선(사진)
메디포스트(078160) 대표가 세포치료제 영토 확장을 통해 제2도약에 나섰다. 메디포스트의 장기인 제대혈을 기반으로 하되 그간 핵심 원료였던 줄기세포에 더해 최근 ‘뜨는’ NK세포(자연살해세포), T세포 등 면역세포를 융합할 계획이다.
양윤선 대표는 5일 경기도 성남시 메디포스트 본사에서 기자와 만나 “제대혈 연구를 오래 하다보니 제대혈에 있는 좋은 면역세포 NK세포와 조절T세포를 활용하면 치료제를 개발할 수 있다는 가능성을 봤다”고 말했다. 조절T세포는 T세포 일종으로 과도한 면역반응을 줄여준다. NK세포는 암세포를 죽이거나 바이러스에 감염된 세포를 제거하는 선천면역세포다.
세포치료제는 세포를 외부에서 배양, 증식, 조작한 뒤 환자에게 주입해 병을 고치는 치료법이다. 항체를 이은 차세대 신약이다. 어떤 세포를 이용하느냐에 따라 다양하다. 메디포스트는 그간 제대혈 유래 줄기세포(중간엽)를 이용한 수술용 무릎 골관절염 세포치료제 ‘카티스템’ 등을 통해 주로 재생(무릎, 발목)을 도모하는 치료제 개발에 주력해왔다. 카티스템은 2012년에 국내에 출시돼 지난해 164억원 매출을 기록, 줄기세포 치료제 중 유일하게 연 매출 100억원을 돌파했다.
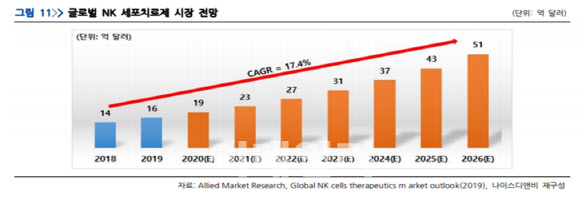 | | (자료=메디포스트) |
|
양윤선 대표는 “조절T세포를 이용해 비정상적인 면역반응이 나타나는 자가면역질환 가운데 콩팥에 염증이 생기는 루푸스신염과 면역이식거부 반응의 하나인 이식편대숙주병 치료제를 개발하려고 한다”며 “면역항암치료제로 개발할 NK세포 치료제는 카티(CAR-T·키메릭 항원 수용체 T세포)의 부작용을 극복할 치료제로 기대를 받고 있다”고 설명했다.
카티는 환자 T세포에 특정한 하나의 암세포를 찾는 일종의 ‘눈’(암세포 특이적인 키메릭 항원 수용체를 발현시키는 유전정보)을 달아 만든 면역세포치료 항암제다. 노바티스의 ‘킴리아’와 길리어드의 ‘예스카타’가 CAR-T 치료제다. 하지만 환자 T세포를 이용해 대량생산이 어려워 고비용인 데다 고형암(혈액암이 아닌 대장암 등)에 쓰기가 어려운 단점이 있다. NK세포 치료제는 대량 복제가 가능한 타인 NK세포를 활용해 CAR-T 대안으로 주목된다. 다만 짧은 약효 시간과 미흡한 대량생산 기술은 넘어야 할 산이다. 아직 상용화된 제품이 없다.
양 대표는 “면역세포도 제대혈에서 얻은 게 성인 말초혈액(혈관에 있는 피)에서 얻는 것보다 증식도 잘하고 특정 질환을 타깃(목표)하기 더 쉽다”며 “그간 카티스템 등을 만들면서 쌓은 줄기세포 치료제 개발 기술을 면역세포 생산과 기능 증진에 활용하면 시너지가 날 것”이라고 강조했다. 제대혈 유래 NK세포를 이용한 세포치료제를 개발하는 곳은 국내에서는 메디포스트와 GC
녹십자랩셀(144510)뿐인 것으로 알려졌다.
그는 고효율의 세포배양플랫폼인 ‘스멉셀(SMUP-Cell)’를 이용한 개방형 혁신도 적극 나설 계획이다. 양대표는 “지난해 말
LG화학(051910)에 생산플랫폼 기술을 이전한 것처럼 유전자 치료제나 마이크로바이옴(장내 미생물 및 유전정보)등 외부 첨단기술과 융합을 해보려고 한다”고 강조했다. 메디포스트는 LG화학에 스멉셀 일부 공정 기술을 총 4278억원 규모(경상기술료 별도)에 이전했다. LG화학은 이 기술에 유전자 기술을 접목해 유전자 세포치료제 개발을 확대할 계획이다.
양 대표는 “단기적으로 주사형 무릎 골관절염치료제(SMUP-IA-01)의 임상을 빨리 진행하려 한다”며 “코로나19 환경에서 속도를 내지 못했던 주요 파이프라인의 국내외 임상을 빠르게 진행하고 기술수출에서도 성과를 내려고 한다”고 했다. SMUP-IA-01의 경우 국내에서 1상까지 마치고 하반기 임상 2상 계획을 제출할 계획이다. 카티스템은 미국에서 임상 3상을 담당할 파트너사를 찾기 위한 기술이전이 모색되고 있다. 말레이시아에서는 최근 카티스템 허가 신청이 들어갔다.
 | | (자료=메디포스트) |
|








![[르포] 안드로이드 탄생한 보스턴CIC가보니…"K-바이오, 빅딜 마중물"](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071401146b.jpg)
![유한양행 ‘렉라자’ 글로벌 매출 급증에 20% ↑…제넥신·국전약품 上[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071800211b.jpg)
![美FDA, 신약 허가 거절시 보완요구서한 공개[제약·바이오 해외토픽]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071900105b.jpg)

