[이데일리 송영두 기자] 이중항체 선두주자로 평가받는
에이비엘바이오(298380)의 신약개발 행보가 주목받고 있다. 최근 바이오젠의 치매치료제가 미국 식품의약국(FDA) 허가를 받으면서, 에이비엘바이오의 퇴행성 뇌 질환 치료제 개발에도 관심이 쏠리는 상황이다. 여기에 올해부터 본격적으로 시작되는 면역항암제에 대한 글로벌 임상도 기대를 모으고 있다.
9일 투자업계(IB)에 따르면 지난 7일 미국 바이오젠이 개발한 퇴행성 뇌 질환 치료제 아두카누맙(알츠하이머)이 미국 식품의약국(FDA)으로부터 치료제로 승인받으면서, 퇴행성 뇌 질환인 파킨슨병 치료제를 개발 중인 에이비엘바이오에 대한 관심도 높아지고 있다. 알츠하이머와 파킨슨은 퇴행성 뇌 질환 중 발병률이 가장 높은 질환으로 꼽히지만, 근본적인 치료제가 없는 상황이다.
김정현 교보증권 연구원은 퇴행성 뇌 질환 치료제를 개발 중인 국내 기업 중 카이노스메드와 함께 에이비엘바이오를 주목해야 할 기업으로 꼽았다. 에이비엘바이오는 이중항체 파킨슨병 치료제 후보물질 ABL301을 개발 중이다. 이중항체 플랫폼 ‘그랩바디-B’가 적용됐고, 임상연구를 통해 우수한 효능도 입증됐다는 게 회사 측 설명이다. 이중항체는 두 개의 항체가 각각 면역세포와 암세포와 붙어 면역세포는 강화하고 암세포는 사멸시키는 기술이다.
에이비엘바이오 관계자는 “ABL301은 전임상 데이터를 통해 반감기와 안전성이 우수한 것으로 나타났으며, 영장류 실험에서도 단독항체 대비 혈액뇌장벽(BBB) 투과율이 13배 높은 것으로 확인됐다”고 말했다. 특히 지난 7일에는 국내 특허도 취득했다. 이상훈 에이비엘바이오 대표는 “파킨슨병 치료제 개발은 현재 전임상 막바지 단계로, 임상에 들어가기 전 최대한 효과성을 확인하기 위해 다양한 전임상을 실시하고 있다”며 “내년 중 국내외 임상을 추진할 계획”이라고 설명했다.
 | | 이상훈 에이비엘바이오 대표.(사진=에이비엘바이오) |
|
이중항체 선두, 떡잎부터 알아본 VC 국내 최고 벤처캐피털(VC)인 한국투자파트너스는 에이비엘바이오 초기 투자를 이끌었다. 한국투자글로벌제약산업육성 사모투자 펀드를 통해 2016년과 2017년 각각 60억원과 50억원을 투자했다. 당시 투자를 이끈 황만순 한국투자파트너스 대표는 회사 설립자와 경영진의 트랙 레코드를 누구보다 중요시한다. 에이비엘바이오는 이상훈 대표의 상징성과 이중항체 기술력에 투자한 것으로 알려졌다.
이 대표는 미국 바이오텍 제넨텍과 한화케미칼,
파멥신(208340)을 거친 국내 신약개발분야 최고 전문가로 평가받는다. 황 대표는 “이 대표는
한화(000880)그룹의 바이오사업을 총괄했었고, 미국 제넨텍과 국내 바이오벤처 파멥신을 이끌었던 경험이 있다. 이중항체에 대한 기술력과 이 대표의 트랙 레코드를 보고 회사 설립과 초기 투자를 제안했었다”고 말했다.
특히 황 대표는 “이중항체 관련 이론은 오래전부터 나왔지만 이를 치료제로 개발하는 등의 사업화를 하는 곳은 드물었다”며 “에이비엘바이오는 이중항체 기반 신약개발에 일찌감치 뛰어들었고, 무엇보다 이 대표의 기술수출 등 사업개발 능력은 국내 최고라고 판단하고 있다. 현재 개발 중인 항암제와 파킨슨병 치료제 등의 성장 잠재력도 높다고 본다”고 강조했다. 한국투자파트너스는 에이비엘바이오가 2019년 4월 코스닥에 상장한 후 일부 지분(3.94%)을 매각해 약 20배 수익을 냈으며, 현재 8.07%(380만4122주) 지분을 보유 중이다.
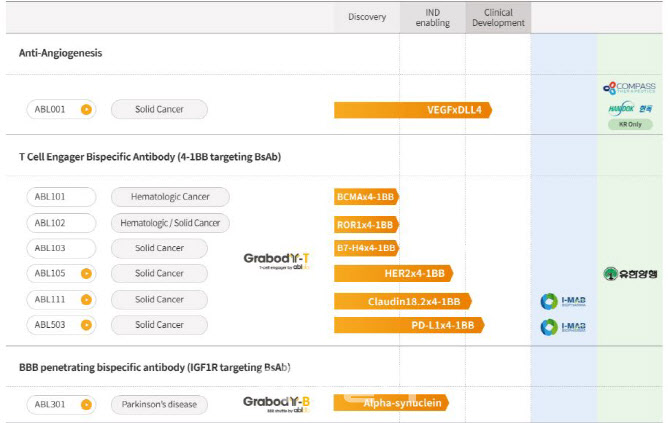 | | 에이비엘바이오 주요 파이프라인.(자료=에이비엘바이오) |
|
본격 성장기 접어든 에이비엘바이오, 新 플랫폼도 개발 중 에이비엘바이오의 이중항체 치료제 핵심 기술은 그랩바디 플랫폼이다. 그랩바디-T와 그랩바디-I는 항암제 전용 플랫폼이고, 글랩바디-B는 퇴행성 뇌 질환 플랫폼이다. 플랫폼을 통해 개발된 후보물질들은 미국 트리거 테라퓨틱스(6649억원 규모),
동아에스티(170900),
유한양행(000100),
한독(002390) 등 국내외 대형 제약사들에 기술이전 됐다.
현재 에이비엘바이오가 개발 중인 이중항체 면역항암제 ABL503은 미국에서 임상 1상을 진행 중이고, 첫 용량 투여군에서 안전성이 확인됐다. 또한 국내에서 개발한 이중항체로는 최초로 국내 임상에 진입한 ABL001은 임상 1상 결과 로슈 블록버스터 치료제 아바스틴 대비 우수한 효능과 안전성이 확인됐다. 올해 하반기 미국 임상시험계획서(IND)를 제출할 예정이고, 중국 임상도 계획하고 있다. 또한 내년 중 추가로 2개의 항암제 후보물질이 미국 임상을 계획하고 있다.
추가적인 기술수출도 기대된다는 분석이다. 진홍국 한국투자증권 연구원은 “면역항암제 후보물질 임상이 본격화 되고 진척을 보이면서 기술수출에 대한 기대감도 여전히 유효하다”고 말했다.
특히 회사는 새로운 항체 플랫폼을 개발하고 기술수출을 추진해 성장해 나겠다는 포부다. 이상훈 대표는 “단순 항체를 탑재하는 플랫폼 구조에서 항체 외에도 펩타이드 등 새로운 물질 탑재가 가능한 플랫폼과 3중 항체 플랫폼을 새롭게 개발 중”이라며 “그동안 전임상 단계 후보물질을 초기에 기술이전 하는 전략을 펼쳤다면, 앞으로는 임상 1/2상 단계의 후보물질을 기술이전하는 전략을 구사할 것이다. 꾸준히 새로운 후보물질들을 임상에 진입시켜 다수의 가치 있는 신약을 보유한 회사로 성장할 것”이라고 말했다.







![고영, 어닝서프라이즈에 '上'…바이젠셀·툴젠도 상승세[바이오맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042700146b.jpg)


![일라이 릴리 10조 베팅·영국 의료 정보 유출[클릭, 글로벌 제약·바이오]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042601061b.jpg)