팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
[이데일리 나은경 기자] 엔데믹으로 주춤하던
지노믹트리(228760)가 방광암·대장암 조기진단키트로 실적 반등을 노린다. 국내 품목허가 절자를 통해 조기진단기기로 인정받아 내년에는 다시 흑자 궤도에 오른다는 계획이다.
8일 금융감독원 전자공시시스템에 따르면 지노믹트리의 지난해 매출은 34억원, 영업손실은 173억원으로 적자전환했다. 2022년에는 매출 299억원, 영업이익 24억원을 냈다. 하지만 엔데믹(감염병의 풍토병화)으로 미국 종속회사의 코로나19 진단 검사서비스 매출이 88.6% 줄어들면서 실적이 고꾸라졌다.
업계에선 올해 있을 여러 모멘텀을 바탕으로 내년에는 다시 흑자 기조로 돌아갈 수 있을 것으로 본다. 연내 대장암 진단키트 ‘얼리텍-C’, 방광암 진단키트 ‘얼리텍-B’의 임상결과가 나오면서 내년부터는 유의미한 매출을 낼 것이란 예측에서다.
간편한 방광암 검진으로 100억 이상 추가 매출 기대 방광암 진단키트 얼리텍-B는 보험 코드 획득 및 매출 본격화라는 모멘텀을 가지고 있다. 현재 국내에서 혈뇨 환자를 대상으로 한 조기진단 기기로 인정받기 위한 대규모 확증임상을 진행 중이다. 최근 1249명의 환자등록을 마쳤는데, 상반기 중에는 식품의약품안전처에 품목허가를 신청하는 것이 가능할 전망이다.
앞서 미국 식품의약국(FDA)으로부터 혁신의료기기로 지정된 얼리텍-B는 미국에서도 대규모 확증임상을 추가 진행해 내년 중 품목허가 및 보험등재를 목표로 한다. 미국 시장 진출시 전사적인 매출 반등도 기대되는 상황이다. 방광암 진단의 글로벌 시장 규모는 2022년 기준 27억 달러(3조5681억원)에서 오는 2030년에는 88억 달러(11조6292억원)까지 성장할 것으로 예상된다.
얼리텍-B는 요도에 내시경을 삽입해 요세포를 관찰해야 했던 기존 방광경 검사 방식과 달리 소변으로 검사가 가능하다는 것이 가장 큰 이점이다. 앞선 임상에서는 민감도 93.2%, 특이도 90.4%를 각각 기록해 대규모 임상에서의 유효성 입증에 대한 기대감이 크다.
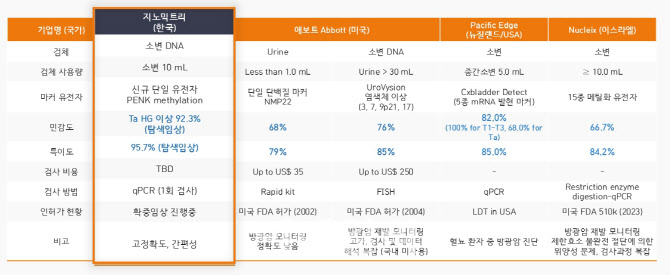 | | 지노믹트리의 방광암 조기진단 제품 ‘얼리텍-B’와 글로벌 경쟁제품 비교 (자료=지노믹트리) |
|
국내에서 연 5000명의 방광암 신규 환자가 발생하는데, 혈뇨 환자의 5~20%가 방광암으로 진단받는다. 이를 감안하면 연간 2만5000~10만명이 잠재적인 얼리텍-B 검사 환자가 될 수 있을 것으로 기대된다. 회사측은 이를 토대로 최소 25억~100억원의 추가 매출이 가능할 것으로 본다.
얼리텍-C, 3월 중 2차 임상 환자등록 완료…반등 예고 이보다 먼저 긍정적인 소식이 기대되는 것은 얼리텍-C다. 지난 2018년 대장암 ‘보조진단’ 의료기기로 허가받은 얼리텍-C는 2019년 국내 출시돼 지난해 4월 신의료기술평가 유예대상으로 선정됐고, 현재 비급여로 사용할 수 있다. 하지만 회사의 당초 목표와 달리 ‘조기진단’이 아닌 ‘보조진단’ 기기로 허가 단계가 격하되면서 신의료기술평가를 받을 수 없었다.
회사는 조기진단 기기로서 신의료기술평가를 받기 위해 대규모 확증임상을 진행 중이다. 총 2340명 모집을 목표로 하는 2차 추가임상은 이달 중 환자 등록이 마무리될 예정이다. 당초 1월 중 환자 등록이 마무리될 것으로 예상됐지만 약 2개월 지연되면서 임상 결과 보고서 수령은 상반기에 가능할 전망이다. 늦어도 내년 초에는 조기진단 기기로의 품목허가 및 보험 등재를 통해 매출 반등을 노린다.
얼리텍-C는 대변 속 DNA 메틸화 바이오마커를 통해 암 환자를 식별하는 분자진단키트다. 지난 2021년 1124명의 대장내시경 검사자를 대상으로한 1차 확증임상에서 민감도 95%, 특이도 87.8%를 입증했다.
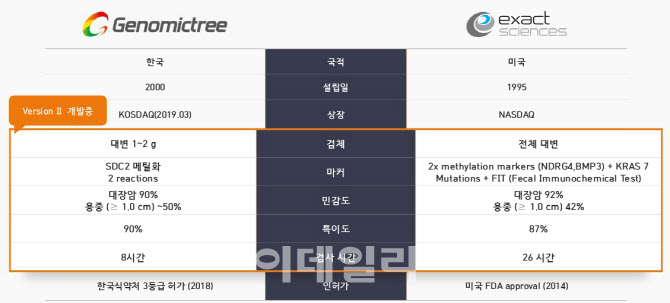 | | 지노믹트리의 대장암 조기진단 제품 ‘얼리텍-C’와 글로벌 경쟁제품 비교 (자료=지노믹트리) |
|
대장암의 경우 조기발견시 90%가 생존할 수 있지만 아직까지는 절반 이상의 환자들이 대장암 말기에 이르러서야 대장암 진단을 받아 매년 사망률이 늘어나는 상황이다. 한송협 대신증권 연구원은 “얼리텍-C로 대장암 조기진단을 통해 사회 전체적인 보건비용을 낮출 수 있다는 점이 증명된다면 높은 가격을 인정받을 수 있을 것”이라고 말했다.
얼리텍-C의 지난해 3분기 누적 매출은 12억원으로 같은 기간 총 매출의 약 44%를 차지했다. 향후 중국, 미국으로도 출시 확대 계획을 갖고 있다. 특히 중국의 경우 내년 품목허가 및 보험 등재를 목표로 한다. 이미 생산시설 구축 및 중국인 검체를 이용한 임상시험을 마쳤고 올 상반기까지 중국내 임상시험이 종료될 예정이다.







![지놈앤컴퍼니, 임상 본격화 기대감에 급등…숨고르기 들어간 바이젠셀[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26043000447b.jpg)


